Изоэлектронность
Cтраница 2
Поскольку теория МО не подчеркивает атомного происхождения электронов в молекуле, она очень удобна для рассмотрения концепции изоэлектронности, широко распространенной в химии. Эта концепция состоит в том, что молекулы, имеющие сходные ядерные конфигурации и одинаковое число электронов, часто обладают близкими свойствами. Прежде всего это относится к таким физическим свойствам, как потенциал ионизации, в меньшей степени это справедливо в отношении реакционной способности. [16]
Поскольку теория МО не подчеркивает атомного происхождения электронов в молекуле, она очень удобна для рассмотрев ния концепции изоэлектронности, широко распространенной в химии. Эта концепция состоит в том, что молекулы, имеющие сходные ядерные конфигурации и одинаковое число электронов, часто обладают близкими свойствами. Прежде всего это отно-сится к таким физическим свойствам, как потенциал ионизации, в меньшей степени это справедливо в отношении реакционной способности. [17]
Все эти соотношения вытекают из единства материальной основы всех атомов ( электроны и положительные ядра) и квантовомеханических законов, а также от изоэлектронности или сходства строения сравниваемых молекул. [18]
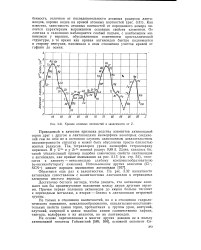 |
Кривая атомных плотностей в зависимости от Z. [19] |
Приводимый в качестве признака родства элементов актиноидной серии друг с другом и лантаноидами изоморфизм некоторых соединений сам по себе не в состоянии служить однозначным доказательством изоэлектронности структур и может быть обусловлен просто близостью ионных радиусов. Так, тетрахлорид урана изоморфен тетрахлориду циркония. [20]
Спектр поглощения антрона ( рис. 42, а) сходен со спектром бензофенона. Это обусловлено изоэлектронностью их хромофорных групп; метиленовый мостик в антроне играет роль алкильного заместителя, слабо влияющего на положение пл - и яя - уровней энергии бензофеноно-вой системы. [21]
Неоднократно постулировалась важность для катализа изоэлектрон-ности валентных оболочек ионов переходных металлов, а также подчеркивалось значение изоэлектроиности бинарных полупроводников с полупроводниками - простыми телами IV группы для возможности появления определенных кристаллохимических и электронных свойств, характерных для полупроводников этой группы. Отсюда следовал естественный вывод о важности их изоэлектронности с Ge, Si и a - Sn для проявления каталитической активности. При этом возможно сохранение тетраэдрической координации, благодаря появлению пробелов или избыточных атомов в одной из частных подре-шеток. [22]
Двухатомные и более сложные молекулы, а также кристаллы, образуемые при различных комбинациях элементов одной и той же строки ( гомо-периодные соединения) или разных строк системы ( гетеропериодные соединения) могут быть рассмотрены с точки зрения учения о ненасыщенности и насыщенности внешних слоев оболочки электронами. Современная наука пользуется теорией недостатка и избытка электронов, а также понятием об изоэлектронности молекул. Следуя за Менделеевым, необходимо пользоваться при этом правилами химического замещения, учением четности и нечетности числа атомных и молекулярных электронов и о пределе насыщения. Подлежит учету и симметрия как электронных оболочек, так и координационных лигандных сфер в молекулах и кристаллах. [23]
Сделанное несколькими годами раньше открытие и объяснение структуры б с-циклопентадиенилжелеза ( II), или ферроцена ( см. гл. Изоэлектронность быс-циклопентадиенилферри-циний-иона и катиона бие-бифенилхрома ( I) ( рис. 8 - 1), принятая теперь во внимание, служила поддержкой ( по крайней мере с теоретической точки зрения) этой наиболее привлекательной гипотезы. [24]
 |
Способность элементов к образованию квасцов. [25] |
Нерастворимый в воде А1РО4 интересен тем, что он имеет структуру кварца. Обусловлено это горизонтальной аналогией, близостью атомных радиусов Al, Si, P, изоэлектронностью. Хорошо растворимый в воде нитрат Al ( NO3) 3 кристаллизуется из воды с 9 молекулами воды. Однако он полностью разрушается в воде. [26]
 |
Способность элементов к образованию квасцов. [27] |
Нерастворимый в воде А1РО интересен тем, что он имеет структуру кварца. Обусловлено это горизонтальной аналогией, близостью атомных радиусов Al, Si, P, изоэлектронностью. Если представить фосфат алюминия в виде АЮ2 - РО2, а диоксид кремния как SiO2 SiO2, то сумма валентных электронов у атома алюминия и фосфора равна 8 и число валентных электронов двух атомов кремния также равно 8, т.е. точно соответствует сумме валентных электронов алюминия и фосфора. [28]
На этой предпосылке основаны корреляции Бильца и Демпси. Идея о том, что почти все карбиды к нитриды можно описать в модели жесткой полосы, положение уровня Ферми в которой изменяется только в зависимости от электронной концентрации или электронного перехода, находит обоснование в поведении сте-хиометрических карбидов и нитридов. Как показывают данные табл. 56, величины у стехиометрических карбидов металлов V и нитридов металлов IV групп, карбидов металлов VI и нитридов металлов V групп соответственно почти равны. Именно эти результаты и обеспечили успех представления об изоэлектронности при коррелировании свойств с плотностью электронных состояний вблизи уровня Ферми в стехиометрических карбидах, нитридах и кар-бонитридах. Для нестехиометрических карбидов и нитридов это предположение не выполняется. Хотя данные о нестехиометрических нитридах весьма ограниченны, все же известно, что изменение их свойств с отклонением от стехиометрии противоположно тому, какое имеет место для нестехиометрических карбидов. Кроме того, исследования рентгеновских спектров показывают, что зонные структуры карбидов и нитридов очень различаются. Следовательно, можно сделать вывод, что рассматриваемое предположение несправедливо. [29]
И в этом случае, для того чтобы появлялись отражения, h, k и I должны одновременно принимать либо четные, либо нечетные значения. Более того, легко видеть, что при четных значениях / г, k и / два члена в правой части равенства (8.6) имеют одинаковый знак, и вклады ионов натрия и хлора будут усиливать друг друга, но при нечетных значениях h, k и I эти члены имеют противоположные знаки и вклады от них будут интерферировать. Поскольку ионы натрия и хлора обладают разными факторами рассеяния, то, хотя все отражения, для которых / г, k и / либо все четные, либо все нечетные, будут появляться, отражения с нечетными индексами будут иметь меньшую интенсивность, чем те, которым соответствуют четные индексы. В кристалле хлористого калия, имеющего такую же структуру, как NaCl, вследствие изоэлектронности, а значит и практически равных факторов рассеяния у ионов калия и хлора, появляются дополнительные особенности. [30]
Страницы: 1 2 3