Дисперсность - коллоидная система
Cтраница 1
Дисперсность коллоидных систем характеризуют размером частиц дисперсной фазы. Так как размеры частиц неодинаковы, то для полного представления о дисперсности необходимо иметь кривую распределения дисперсной фазы по размерам частиц, которую строят по данным дисперсионного анализа. Последний осуществляют седиментационным методом или методом микроскопи-рования. [1]
Дисперсность коагулированной коллоидной системы можно восстановить, добавляя специальные адсорбирующие вещества - пептизаторы. Процесс восстановления дисперсности в этом случае носит название пептизации. Пептизатор, адсорбируясь на поверхности частиц дисперсной фазы, действует как стабилизатор. [2]
Степень дисперсности коллоидных систем характеризуется обычно линейными размерами частиц: чем больше размер частиц, тем меньше степень дисперсности и наоборот. [3]
Верхний предел дисперсности коллоидных систем обусловлен тем, что при даль - нейшем дроблении вещества в растворе уже будут находиться не агрегаты молекул, а отдельные молекулы, имеющие размер порядка 0 1 нм. Нижний предел дисперсности коллоидных систем определяется резким снижением интенсивности теплового движения частиц поперечным размером больше 100 нм. Несмотря на установленный предел в 100 нм в курсе коллоидной химии рассматриваются обычно и более грубодисперсные системы, размер частиц которых может достигать несколько микрометров, а иногда и значительно больше. [4]
Верхний предел дисперсности коллоидных систем обусловлен тем, что при дальнейшем дроблении вещества в растворе уже будут находиться не агрегаты молекул, а отдельные молекулы, имеющие размер порядка 0 1 нм. Нижний предел дисперсности коллоидных систем определяется резким снижением интенсивности теплового движения частиц поперечным размером о Ьльше 100 нм. [5]
 |
Изменение уд при дроблении 1 см3 вещества. [6] |
С повышением дисперсности коллоидной системы ее удельная поверхность резко возрастает. [7]
 |
Изменение яуд при дроблении Г см3 вещества. [8] |
С повышением дисперсности коллоидной системы ее удельная поверхность резко возрастает. Это видно из табл. 1 1, в которой показано изменение удельной поверхности 1 см3 вещества при дроблении его на кубики меньших размеров. [9]
Верхний предел дисперсности коллоидных систем обусловлен тем, что при даль - нейшем дроблении вещества в растворе уже будут находиться не агрегаты молекул, а отдельные молекулы, имеющие размер порядка 0 1 нм. Нижний предел дисперсности коллоидных систем определяется резким снижением интенсивности теплового движения частиц поперечным размером больше 100 нм. Несмотря на установленный предел в 100 нм в курсе коллоидной химии рассматриваются обычно и более грубодисперсные системы, размер частиц которых может достигать несколько микрометров, а иногда и значительно больше. [10]
 |
Изменение яуд при дроблении Г см3 вещества. [11] |
С повышением дисперсности коллоидной системы ее удельная поверхность резко возрастает. Это видно из табл. 1 1, в которой показано изменение удельной поверхности 1 см3 вещества при дроблении его на кубики меньших размеров. [12]
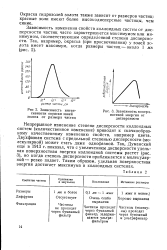 |
Зависимость поверхностной энергии от дисперсности. [13] |
Непрерывное изменение степени дисперсности коллоидных систем ( количественное изменение) приводит к скачкообразному качественному изменению свойств, например цвета. Двухфазная система с предельной степенью дисперсности ( молекулярной) может стать даже однофазной. Так, Думанский еще в 1913 г. показал, что с увеличением дисперсности удельная поверхностная энергия коллоидной системы растет ( рис. 3), но когда степень дисперсности приближается к молекулярной-резко падает. Таким образом, удельная поверхностная энергия достигает максимума в коллоидных системах. [14]
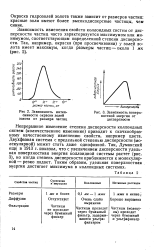 |
Зависимость поверхностной энергии от дисперсности. [15] |
Страницы: 1 2 3