Изучение - кинетика - окисление
Cтраница 1
Изучение кинетики окисления и распада ацетальдегида на ванадиевых катализаторах показало, что в условиях окислительного катализа углеводородов альдегиды окисляются и распадаются значительно быстрее, чем исходный углеводород. Поэтому трудно осуществить накопление ценных продуктов окисления. Кроме того, на катализаторах VaOe, серебре и др. наблюдается адсорбция альдегидов, протекающая с большой скоростью при температурах катализа. Аналогичные данные получены и для формальдегида. [1]
Изучение кинетики окисления касается двух основных факторов: общей скорости реакции и промежуточных продуктов, череа которые происходит превращение углеводородов в конечные продукты окисления. Такое превращение не является процессом, протекающим, в одну стадию и зависящим от одной определяющей его скорость реакции, а представляет собой ряд последовательных стадий, зависящих от многих влияющих на скорость факторов. В связи с тем, что реакция окисления состоит из ряда индивидуальных стадий, усилия исследователей были направлены на выделение каждой стадии и объяснение конечных результатов в соответствии с данными, полученными по каждой отдельной реакции. [2]
Изучение кинетики окисления дифенилсульфоксида до суль-фона надбензойной и надуксусной кислотами, проведенное Цмантом и другими исследователями142, привело их к выводу, что механизм реакции аналогичен предложенному ранее для окисления олефинов, оксимов и фенилгидразонов. [3]
Изучение кинетики окисления толуола хромовым ангидридом в уксусной кислоте до бензойной кислоты также показало, что в процессе участвуют 2 мол. [4]
Изучение кинетики окисления этилбензола в присутствии аминов и фенольных соединений [5] показало, что в процессе окисления концентрация амина в смеси остается постоянной вплоть до полного расходования фенола. Это, вероятно, связано с тем, что при окислении амина образуется свободный радикал, который отрывает атом водорода от молекулы фенола, давая новую молекулу амина; вследствие этого концентрация амина практически не меняется до тех пор, пока не израсходуется весь фенол. [5]
Изучение кинетики окисления этилбензола в присутствии аминов и фенольных соединений52 показало, что в процессе окисления концентрация амина в смеси остается постоянной вплоть до полного расходования фенола. Это, вероятно, связано с тем, что при окислении амина образуется свободный радикал, который отрывает атом водорода от молекулы фенола, давая новую молекулу амина; вследствие этого концентрация амина практически не меняется до тех пор, пока не израсходуется весь фенол. [6]
Изучение кинетики окисления дифенилсульфоксида до суль-фона надбензойной и надуксусной кислотами, проведенное Цмантом и другими исследователями142, привело их к выводу, что механизм реакции аналогичен предложенному ранее для окисления олефинов, оксимов и фенилгидразонов. [7]
Изучение кинетики окисления различных восстановленных катализаторов синтеза аммиака показывает их высокую активность в реакциях с водяным паром при 900 С. [8]
Изучению кинетики окисления углеродистых отложений да неорганических катализаторах кислородом воздуха посвящено большое число работ [33, 43-45, 47-53], решивших ряд важных технологических проблем регенерации промышленных катализаторов. [9]
Изучению кинетики ларофазного окисления нафталина уделялось мало внимания. Он установил, что в этих условиях 1 4-нафто-хинон образуется быстрее, чем фталевый ангидрид, и что энергия активации обеих реакций одинакова ( 26 / скал), и пришел к выводу, что стадия, определяющая скорость этих реакций, одна и та же; вероятно, это - хемосорбция кислорода катализатором. Таким образом, нафтохинон не является промежуточным продуктом окисления нафталина во фталевый ангидрид в указанных условиях, которые, конечно, совершенно отличны - от применяемых в технике. [10]
Для изучения кинетики окисления металлов применяется метод периодического взвешивания образца без извлечения его из печи. Схема такой установки представлена на фиг. Испытываемый образец 2 подвешивается к чашке аналитических весов на тонкой нихромовой проволоке 6, пропущенной через отверстие в изолирующем экране и в крышке 5 электропечи. Образец нагревается в рабочем пространстве электропечи. [11]
Однако изучение кинетики окисления нафталина в присутствя 7йОй показало, что гетерогенное окисление нафталина, как и ДР гих ароматических углеводородов, состоит из нескольких пара-дельных и параллельно-последовательных реакций. [12]
Проведено изучение кинетики окисления титана марки ВТ-1Д в интервале температур 800 - 1150 С в газовых смесях О2 - f N2 различного состава. Показано, что при выдержках более одного часа окисление во всем исследованном интервале температур следует по линейному закону. [13]
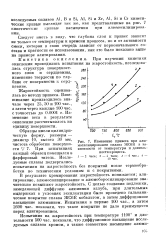 |
Изменение привеса при алю-мосилицированип сплава ЖС6К в зависимости от температуры п длительности процесса. [14] |
При изучении кинетики окисления проводились испытания на жаростойкость, исследовалась структура поверхностного слоя и сердцевины, изменение твердости по глубине от поверхности к сердцевине. [15]
Страницы: 1 2 3 4