Изучение - кинетика - окисление
Cтраница 2
При изучении кинетики окисления углеводородов большое внимание было уделено анализу характера зависимости реакционной способности от строения различных классов углеводородов. [16]
При изучении кинетики окисления металла в газовой среде применяют метод периодического взвешивания, для чего испытуемый образец подвешивают к одному из концов коромысла аналитических весов и выдерживают в печи при определенной температуре в потоке газа заданного состава. [17]
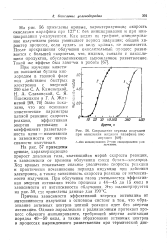 |
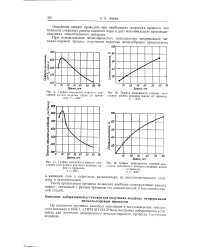
Сокращение периода индукции при окислении жидкого парафина кислородом. [18] |
При изучении кинетики окисления бутана кислородом в газовой фазе под действием быстрых электронов с энергией 200 кэв С. А. Каменецкой, Н. А. Славинской, С. Я. Пшежецким и Г. А. Жит-невой [69, 70] было показано, что все основные кинетические параметры цепной реакции: скорость реакции, эффективная энергия активации и коэффициент разветвленное цепи - изменяются в зависимости от интенсивности излучения. [19]
При изучении кинетики окисления никеля установлено, что скорость окисления возрастает с увеличением давления кислорода. [20]
При изучении кинетики окисления гидрохинона обнаружено влияние образующейся твердой фазы продуктов реакции на кинетику данного процесса. [21]
При изучении кинетики окисления реакции проводят в темных склянках или используют термостатические жидкости, окрашенные красителем в темный цвет, чтобы исключить возможность попадания света в склянки. Выбор окислителя, рН реакционной смеси и растворителя проводят в соответствии со сказанным выше. При приготовлении реакционного раствора нужно смешивать разбавленные растворы, так как реакции неспецифического окисления более легко протекают в концентрированных растворах и, следовательно, разбавление позволит их избежать. Образец растворяют в воде или буферном растворе и добавляют равный объем раствора, в котором концентрация периодата в два раза выше, чем это необходимо по расчету. Для определения большинства кинетических характеристик достаточно трехкратного избытка периодата, однако в случае необходимости можно попытаться использовать и двадцатикратный избыток периодата. [22]
В результате изучения кинетики окисления и состава образующихся при этом продуктов вполне очевидно, что все сераоргани-ческие соединения при определенных концентрациях тормозят окисление ИПБ. Торможение цепной реакции окисления происходит в результате взаимодействия сераорганических соединений с гидроперекисью ИПБ. [23]
На основании изучения кинетики окисления и восстановления смешанного контакта в 1954 г. в ИГИ АН СССР была построена лабораторная установка для изучения непрерывного металло-парового процесса получения водорода. [25]
На основании изучения кинетики окисления метановых, нафтеновых и ароматических углеводородов составляющих керосиновые фракции, В. К. Цысковский [117] делает заключение, что в случае каталитического окисления сложной смеси этих углеводородов при приблизительно равной величине молекулы наивысшей химической активностью обладают все ароматические углеводороды, затем нафтеновые и, наконец, метановые. Он также утверждает, что нафтеновые углеводороды, в случае окисления их при высоких температурах, оказались активнее не только метановых, но ь ароматических углеводородов. [26]
Отсюда вытекает целесообразность изучения кинетики окисления и смолообразования топлив для разработки способов их стабилизации. [27]
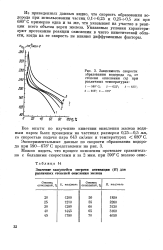 |
Зависимость скорости образования водорода Ун2 от степени окисления ( т при различных температурах. [28] |
Все опыты по изучению кинетики окисления железа водяным паром были проведены на частицах размером 0 25 - 0 5 мм, со скоростью подачи пара 643 см / мин и температурах 680 С. [29]
Общим недостатком при изучении кинетики окисления коксовых отложений на катализаторах является узкий интервал варьирования определяющих параметров: начальной степени закоксованности, концентрации кислорода и особенно температуры. Кинетические уравнения составлялись на основе гипотез о механизме, которые не учитывают даже хорошо установленные факты многостадийности окисления [3, 92], когда на первой стадии образуется промежуточный поверхностный комплекс углерода с кислородом. [30]
Страницы: 1 2 3 4