Изучение - кинетика - реакция
Cтраница 2
Изучение кинетики реакции показало, что она протекает как 5в2 - замещение у насыщенного атома углерода. [16]
Изучение кинетики реакции в пламени осложняют трудности изменения только одного из кинетических параметров. Так, изменение состава горючей смеси и общего давления во многих случаях влечет за собой и изменение температуры горения. Необходимы специальные методы, позволяющие варьировать только один изучаемый параметр при постоянстве остальных. [17]
Изучение кинетики реакций в проточных системах, в отличие от систем статических ( аппараты периодического действия), имеет свои особенности. Основная разница в исследовании кинетики этих двух методов проведения процесса обусловлена вопросом о том, как учитывать время пребывания реактантов в зоне реакции, от которого зависит глубина превращения исходного сырья. [18]
Изучение кинетики реакций, в которых участвуют твердые вещества, имеет не только теоретическое, но и большое практическое значение. Большинство реакций, имеющих значение для техники, протекает с участием твердых веществ. [19]
Изучение кинетики реакции между AgBr, AgJ - Ag2S3, Sb2S3 показало, что в этих случаях изменение скорости реакции с разбавлением значительно меньше тех изменений, которые можно было бы ожидать исходя из предположения, что реакция протекает путем соударения частиц. [20]
Изучение кинетики реакции показало, что в противоположность борогидридному восстановлению вхождение в анион алкоксигруп-пы уменьшает восстановительную способность алюмогидрида, и поэтому каждая последующая стадия передачи гидрид-иона проходит медленнее предыдущей, так что самой быстрой стадией оказывается первая. При этом передача гидрид-иона на каждой из стадий облегчается координацией карбонильного атома кислорода с катионом металла, которая поляризует карбонильную группу, вследствие чего глубина восстановления зависит от координирующих свойств катиона металла. Можно полагать, что катион лития из-за меньшего размера поляризует карбонильную группу больше, чем катион натрия, и поэтому гидрид-ион более легко переносится от алюминия к углеродному атому в случае L1A1H4, чем NaAlH Это вполне согласуется с их относительной реакционной способностью, отмеченной выше. [21]
Изучение кинетики реакций циркуляционным методом осуществляется по принципу статического метода, но с перемешиванием реакционной системы над катализатором путем циркуляции. Этим достигается возможность легкого устранения внешне-диффузионных факторов и при давлениях, более высоких, чем обычно применяемые в статической системе. [22]
Изучение кинетики реакции на катализаторе в адсорбированном-слое представляет собой важный частный случай применения статического метода. При этом исходные вещества, или по крайней мере одно из них, берутся в количествах, целиком адсорбирующихся на поверхности катализатора. Реакционная система выбирается так, чтобы хотя бы один из продуктов реакции или одно из исходных веществ практически не адсорбировалось на катализаторе. Тогда о ходе реакции можно судить по поглощению исходного вещества из газовой фазы в результате его взаимодействия с другим адсорбированным веществом и образованием адсорбированных продуктов реакции или же по выделению образующегося продукта, практически не адсорбирующегося на поверхности. [23]
Изучение кинетики реакции часто давало много сведений о ее механизие. [24]
Изучение кинетики реакций этерификации и омыления, начатое впервые Вертело ( 1862), является одним из классических примеров физико-химического исследования, оказавшим сильное влияние на развитие физической химии. [25]
Изучение кинетики реакции конденсации Ц пклогексапона представляет значительны. [26]
Изучение кинетики реакций этерификации и омыления, начатое впервые Вертело ( 1862), является одним из классических примеров физико-химического исследования, оказавшим сильное влияние на развитие физической химии. [27]
Изучение кинетики реакций нитрования о - и я-нитрофенола, а также 2 4-и 2 6-динитрофенола избытком 10 - 60 % - ной азотной кислоты показало, что все эти реакции катализируются азотистой кислотой. При определенной концентрации азотной кислоты скорость реакции прямо пропорциональна концентрации нитруемого соединения и азотистой кислоты. [28]
Изучение кинетики реакции ряда ароматических хлорпроизводных с растворами аммиака в присутствии соединений меди показало 40, что в этом случае скорость реакции прямо пропорциональна концентрации хлорпроизводного и катализатора и не зависит от концентрации аммиака. [29]
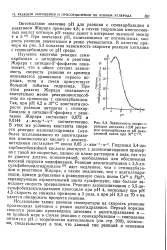 |
Зависимость скорости реакции цитидина с2М раство. [30] |
Страницы: 1 2 3 4