Адсорбция - ингибитор
Cтраница 1
Адсорбция ингибитора на поверхности металла может повысить его ингибирующую активность. Именно так поверхность меди воздействует на ионол, повышая его активность по отношению к пероксидным радикалам примерно на порядок. [1]
Адсорбция ингибитора твердой фазой гидратирупцихся цементов выражается в изменении концентрации добавки в вытяжке из инги - бированной суспензии по сравнению с количеством, введенный в воду затворения при приготовлении тампонажного раствора. [2]
Адсорбция ингибиторов на поверхности В снижает скорость реакции до скорости, свойственной поверхности А, и в результате обе поверхности травятся однотипно. [3]
Адсорбция ингибитора на твердом металлическом электроде зависит от его потенциала коррозии в коррозионной среде, структуры металла, типа обработки поверхности, механических нагрузок и других факторов. [4]
Адсорбция ингибиторов на поверхности металла происходит в двойном электрическом слое. На их адсорбцию существенно влияют величина и знак заряда металлической поверхности. Адсорбция нейтральных молекул ингибитора определяется силами межмолекулярного взаимодействия ( силы Ван-дер - Ваальса); ври. [5]
Адсорбция ингибиторов на поверхности металла может иметь различную природу. [7]
Адсорбция непредельных ингибиторов на поверхности переходных металлов может происходить не только за счет донорно-акцепторного взаимодействия, когда электроны я-связи переходят на вакантные орбитали металла. Определенную роль в адсорбции должен играть и такой механизм взаимодействия ингибиторов с поверхностью металла, когда электроны переходят на вакантные орбитали С С - или С С-связей. [8]
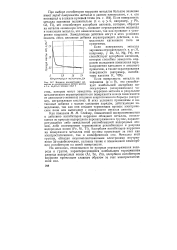 |
Влияние концентрации желатина на коррозионные потери железа в 2 - н. Н25О4в течение 22 5 ч. [9] |
Адсорбция ингибиторов коррозии на поверхности металлов этой группы происходит за счет как электростатических, так и специфических сил. [10]
 |
Примерная схема подводного подключения кабеля. [11] |
Для адсорбции ингибиторов поверхностью металла они должны иметь в своей структуре поверхностно-активные группы, замедляющие электрохимические реакции. [12]
При адсорбции заряженных ингибиторов явления резко усложняются вследствие изменения строения двойного электрического-слоя. [13]
При адсорбции ингибитора коллоидного типа из водной среды на поверхности металла при концентрации выше ККМ образуются не моно -, а сразу бимолекулярные слои молекул. Это отвечает минимальной разности полярности соприкасающихся фаз. Если первый слой ингибитора формируется с помощью мицеллярных частиц с солюбилизированным в них углеводородом, то его строение можно уподобить строению пластинчатой мицеллы ( см. рис. 35, / - 2), нижняя часть которой хемосорбционно фиксирована на металлической поверхности. Между противоположно ориентированными слоями этой мицеллы заключено равновесное количество солюбилизированного углеводорода. [14]
Степень адсорбции ингибиторов поверхностью металла зависит от нескольких свойств металла, главные из которых: потенциал точки нулевого заряда металла, знак заряда поверхности, способность оксидных пленок металлов к ионообменным реакциям с ионами ингибиторов. [15]
Страницы: 1 2 3 4