Адсорбция - компонент
Cтраница 2
FJ - адсорбция компонента; а, - активность этого компонента в растворе. [16]
Данные по адсорбции компонентов солюбилизированных систем на гидрофильных адсорбентах очень немногочисленны. [18]
Поскольку коэффициенты адсорбции компонентов различны, зоны движутся с разной скоростью. В случае неравновесности адсорбции, вызванной внутренней или внешней диффузией или же кинетикой самого процесса адсорбции, в уравнение движения хроматографической зоны вводится величина, характеризующая запаздывание достижения равновесной адсорбции. [19]
Парциальные изотермы адсорбции компонентов до равновесной концентрации 0 8 ммолъ / кг ( в 0 3) одинаковы, что обусловлено равными значениями - AF компонентов. Дальнейшее различие изотерм адсорбции связано с особенностями поведения молекул компонентов в адсорбционном объеме при их высокой поверхности концентрации. Эти различия учитываются коэффициентами активности в адсорбционной фазе. [21]
В результате адсорбции компонентов среды при W & M Wо ( случай образования соединений устойчивой валентности) происходит торможение ионизации металла. [22]
Представление о нелокализованной адсорбции компонентов раствора основано на том, что при дисперсионной природе адсорбционных сил не отдельные центры на поверхности, а каждый атом поверхности адсорбента участвует во взаимодействии с атомами адсорбированных молекул. [23]
Представление о нелокализованной адсорбции компонентов раствора основано на том, что при дисперсионной природе адсорбционных сил не отдельные центры на поверхности, а каждый атом поверхности адсорбента участвует во взаимодействии с атомами адсорбированных молекул. Поэтому в пределах поля действия адсорбционных сил молекулы сохраняют подвижность и в адсорбционной фазе ведут себя по существу так же, как и в растворе соответствующего состава, отличаясь лишь меньшими значениями коэффициентов диффузии и характером взаимодействия между собой вследствие навязанной полем адсорбента их однотипной ориентации на границе раздела с полярным растворителем. [24]
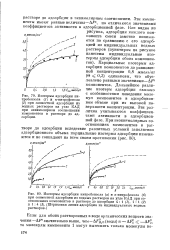
При изучении адсорбции компонентов солюбилизированных систем на ацетиленовой саже [23, 24] было установлено ( рис. 39 - 41), что адсорбция из растворов, солюбилизировавших как нафталин, так и краситель, существенно ниже ( на 10 - 37 %), чем из растворов ПАВ, не содержащих солюбилизированных веществ. Влияние солюби - никнуть как результат конкуренции молекул ПАВ и молекул углеводородов или красителя за свободные места на поверхности раздела фаз, обусловленной различием в величинах уменьшения свободной энергии адсорбции ПАВ и молекул солю-билизата. [25]
Здесь А - адсорбции компонентов; ц - их химические потенциалы, a Ni - мольные доля в объеме раствора. Иначе говоря, концентрация компонента в поверхностном слое ( N) равна его мольной доле ( N) в объеме. [26]
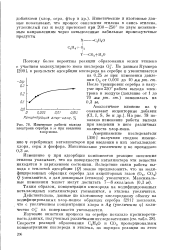 |
Изменение работы выхода. [27] |
Изменение ф при адсорбции компонентов реакции окисления этилена указывает, что на поверхности катализатора эти вещества находятся в заряженном состоянии. Вследствие связи работы выхода с теплотой адсорбции ( Q) можно предположить, что на модифицированных образцах серебра для акцепторных газов ( 02, С02) Q уменьшится, а для доннорных ( этилена) увеличится. [28]
Определение истинной изотермы адсорбции компонента А на С, по которой можно найти емкость мономолекулярного слоя ат и далее по формуле ( 22) найти 5УД, - операция длительная и трудоемкая. Обычно используют раствор сильно адсорбирующегося вещества А в слабо адсорбирующемся растворителе. В этом случае на поверхности сорбента образуется плотный слой преимущественно из молекул А, и адсорбцию можно считать практически мономолекулярной. [29]
Это отклонение объясняется адсорбцией компонентов смеси на стенках камеры при высоких концентрациях и последующей медленной десорбцией. [30]
Страницы: 1 2 3 4