Изучение - кинетика - адсорбция
Cтраница 1
Изучение кинетики адсорбции при разных температурах позволяет найти величину энергии активации процесса адсорбции органического вещества. [2]
Изучение кинетики адсорбции в чистом виде - задача крайне сложная, так как наблюдаемое поглощение вещества на межфазной границе протекает в два этапа: 1) диффузия вещества к поверхности и 2) собственно адсорбция. Очень часто кинетику наблюдаемого процесса определяют преимущественно диффузионные явления. [3]
Изучение кинетики адсорбции в чистом виде - задача крайне сложная, так как наблюдаемое поглощение вещества на границе фаз протекает в два этапа: 1) диффузия вещества к поверхности; 2) собственно адсорбция. Очень часто кинетику наблюдаемого процесса определяют преимущественно диффузионные явления. В пористых адсорбентах могут существовать два режима диффузионных процессов: внешнедиффузионный и внутридиффузионный. В первом скорость переноса вещества определяется переходом его из объема жидкости к входу в капилляр, причем внутри капилляра концентрации принимаются равновесными. [4]
 |
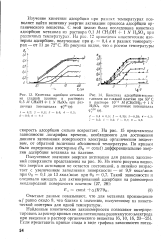
Изотермы адсорбции азота, воды и бензола на кадмиевых цеолитах типа X. На образце натриевого цеолита изучалась адсорбция азота и бензола. [5] |
Изучение кинетики адсорбции на цеолитах привлекает внимание исследователей. [6]
Изучение кинетики адсорбции ПАВ может быть рекомендовано для использования на практике в качестве метода определения механизма действия ингибиторов кислотной коррозии. Даже с учетом ограничений, вытекающих из использования представлений только-о двух типах механизма и трех видах изотерм адсорбции, получаемые результаты представляют интерес, особенно при исследовании технических ингибиторов. Определение механизма действия ингибитора дает возможность подойти к решению вопроса о повышении эффективности защиты путем изменения состава ингибитора или кислотной среды. Время окончания адсорбции или достижения ингибитором определенной степени торможения электродного процесса дает информацию о технологических особенностях применения данного ПАВ для тех или иных производственных целей. [7]
Изучение кинетики адсорбции фосфина проводилось большей частью при давлении 110 мм рт. ст. Указанное давление было выбрано для получения больших абсолютных значений активированной адсорбции фосфина. [8]
 |
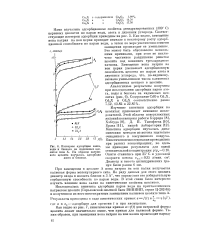
Кинетические кривые адсорбции паров воды на натриевом и водородных цеолитах типа X. [9] |
Изучение кинетики адсорбции паров бензола ( рис. 10) и сравнение с данными по кинетике адсорбции паров воды позволяют сделать следующее заключение. [10]
При изучении кинетики адсорбции из растворов как одной из стадий каталитических реакций представляют интерес два вопроса: 1) взаимосвязь величины поверхностной концентрации растворенных веществ с их объемной концентрацией п 2) определение физических характеристик сорбционного состояния молекулы на поверхности при наличии жидкой фазы в объеме. [11]
При изучении кинетики адсорбции цеолитами определение коэффициентов внутрикристаллической диффузии в цеолитах существенно осложняется влиянием массопереноса в транспортных порах и тепловыми эффектами. При этом если составляющую диффузии в транспортных порах можно сделать преяебрежимо малой, уменьшая размер гранулы или слоя и увеличивая размер кристаллов, то тепловую составляющую устранить таким образом невозможно. [12]
При изучении кинетики адсорбции в ограниченном объеме, так же как и при проведении опытов при постоянной концентрации адсорбтива, для вычисления тг и та необходимо решить систему двух уравнений с двумя неизвестными. Для этого надо знать либо первый ( М) и второй ( Мг) моменты кинетической кривой, либо первые моменты ( М 4 и М Л для двух зерен адсорбента различного размера или различной формы. [13]
При изучении кинетики адсорбции важно определить либо время достижения равновесия, когда удаляемый компонент насытил адсорбент и его концентрация в проходящем компоненте остается постоянной, либо степень обогащения, достигаемую при отделении адсорбента от внешней жидкости через определенное время. Время достижения равновесия устанавливают экспериментально, отбирая пробы через определенные промежутки времени. [14]
При изучении кинетики адсорбции w - бутиламина и пиридина, как и в случае аммиака, обнаружено медленное установление теплового равновесия. Однако механизм медленных процессов для этих оснований, по-видимому, различен. На цеолите NaY бутиламин адсорбируется быстро. При деалюминировании число катионов в больших полостях уменьшается и после их заполнения начинается медленное взаимодействие с катионами, диффундирующими из малых полостей. [15]
Страницы: 1 2 3