Адсорбция - атом
Cтраница 1
Адсорбция атомов на поверхности может привести к существенным изменениям картины реконструисвдии и электронных поверхностных состояний, поскольку адсорбированные атомы вступают в химическую связь с гибридизованными ор-биталями оборванных связей. Рассмотрим модель, в которой каждый атом водорода находится над одним из поверхностных атомов и вступает в химическую связь с гибридизованной орбиталью оборванной связи этого атома. При этом связывающее состояние рассматриваемого поверхностного атома оказывается занятым двумя электронами, что приводит к устранению причины реконструкции. Такая модель согласуется с экспериментами Айбаха и Роу, в которых они обнаружили, что манослой адсорбированных атомов приводит к исчезновению сверхструктуры ( 2X1) на реконструированной поверхности, и с их объяснением этого явления. [1]
Адсорбция атома на поверхности сопровождается изменениями в электронном состояний приповерхностного слоя твердого тела. Это объясняется сложностью природы химических связей, трактовка которых требует решения трудных квантово-химических задач, для которых данные о квантовых состояниях изолированных атомов и молекул оказываются совершенно недостаточными. [2]
Адсорбция атомов азота на железном катализаторе и ионов цезия на поверхности вольфрама является примером хемосорбции. [3]
Адсорбция атома V группы происходит, по-видимому, следующим образом ( см. работу Ландера и Моррисона [252]): атом образует химические связи с тремя соседними поверхностными атомами кремния, а оставшиеся два электрона этого атома о б-разуют ги бриди зованное состояние оборванной - связи. По такой схеме происходит, например, адсорбция атомов фосфора. Аналогичная ситуация имеет место и при адсорбции алюминия, являющегося элементом III группы, с той лишь разницей, что - гиб-ридизованное состояние оборванной связи у этого атома остается незаполненным. Межатомное ( расстояшщ в таком мостике равно межатомному расстоянию в молекуле, хотя углы между связями имеют другое значение. В действительности атом может расположиться над тремя поверхностными атомами двумя различными способами. В первом случае адсорбированный атом располагается прямо над поверхностным атомом, а во втором случае - сбоку от него. Kipowe того, тот факт, что нецентральная силовая постоянная С значительно меньше центральной силовой постоянной С0 ( это особенно проявляется в ионных полупроводниках), показывает, что на поверхности полупроводника энергетически наиболее выгодным типом деформации является изменение углов между связями. [4]
 |
Схема строения ческих реакций, совершающихся на элек. [5] |
При адсорбции атомов кислорода картина меняется. Адсорбированные атомы представляют собой диполи, прочно. [6]
При адсорбции атома натрия на поверхности вольфрама он переходит в ион. Теплота адсорбции может быть определена из рис. 5 ( раздел V, 8а) как разность между уровнем А ( атомное состояние) и минимумом Е на кривой DEF. Энергетическая разность между уровнями D и Е определяется в основном уравнением ( 16) с поправками на силы Ван-дер - Ваальса, поляризационные силы и силы отталкивания. Суммарная величина энергетической разности ( Qi) составляет примерно 77 ккал / моль. [7]
При адсорбции атома натрия на поверхности вольфрама он переходит в ион. Энергетическая разность между уровнями D и Е определяется в основном уравнением ( 16) с поправками на силы Ван-дер - Ваальса, поляризационные силы и силы отталкивания. Суммарная величина энергетической разности ( Q, ) составляет примерно 77 ккал / моль. [8]
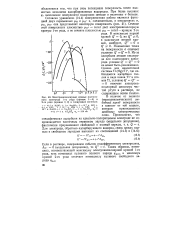 |
Электрокапиллярные кривые платинового электрода 1-го рода ( кривые / - 4 и 2-го рода ( кривые 5, 6 в следующих системах. [9] |
Из-за адсорбции атомов кислорода для платинового электрода условие Q Q О не может быть реализовано. Однако для аналогичной системы Tl ( Hg) / Tl, где наблюдается адсорбция таллия в виде ионов ТГ и атомов Т1, условию Q Q 0 отвечает электрокапиллярный максимум чистой ртути в растворе, не содержащем ионов таллия. [10]
 |
Схема строе - ских реакций, совершающихся на электро. [11] |
При адсорбции атомов кислорода картина меняется. [12]
 |
Схема строения двойного электрического слоя. [13] |
При адсорбции атомов кислорода картина меняется. Поэтому отрицательные полюса атомов кислорода уменьшают положительный ( или увеличивают отрицательный) заряд металлической обкладки двойного слоя. Очевидно, что переход от строения двойного слоя, изображенного на рис. 68, а, к изображенному на рис. 68, б сопровождается изменением градиента потенциала в плотной части двойного слоя. [14]
Усиление адсорбции модифицирующих атомов на докритических зародышах вызывает понижение поверхностного натяжения на их границе с переохлажденным расплавом, вследствие чего они становятся критическими при меньших переохлаждениях. [15]
Страницы: 1 2 3 4