Адсорбция - органическая молекула
Cтраница 3
В § 2 будет дана математическая постановка задачи, в § 3, 4 рассмотрено влияние на фотоэмиссионный ток я) / - потенциала, специфической адсорбции анионов и катионов, а также адсорбции органических молекул с длинной углеводородной цепью. Проведенное далее сравнение теории с экспериментом иллюстрирует возможности фотоэмиссионного метода исследования структуры двойного слоя. Наконец, в § 5 рассмотрен вопрос о роли неоднородности поверхности электрода и найдена зависимость фототока от степени покрытия поверхности адсорбатом. При этом ряд полученных результатов может быть обобщен на более широкий класс электронных переходов. [31]
Таким образом, представляется, что общее замедляющее действие органических веществ включает также потенциальное ускорение начальной стадии гидратации, чему способствует комплексообразование с участием алюминатов и последующее замедление процессов гидратации благодаря стабилизации гексагональных фаз за счет адсорбции органических молекул на поверхности гидратов и образованию на их поверхности защитных пленок. Отмечено [57], что такие органические добавки-водопонизители, как глюкоза, молочная, глюконовая и малоновая кислоты, тормозят превращение гексагональных гидроалюминатов в СзАНе кубический за счет стабилизации гексагональных фаз. Через сутки при 60 С и 75 % - ной влажности СзАНп полностью превращается в СзАНе и Са ( ОН) 2, тогда как при относительной влажности 33 % наблюдается лишь частичное фазовое превращение. При введении в эту систему органической добавки наблюдается возрастание базальных расстояний, что характерно для поверхностных соединений. [32]
 |
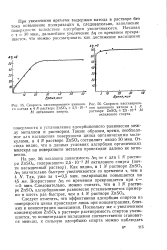
Кривая пассивирования цинкового катода, полученная в 2 N ZnSQi с добавкой октилового спирта ( 0 0115 М при iK 2 ма /. [33] |
В совместной работе с Н. Т. Ваграмян [13], в которой учитывалась истинная плотность тока, нами было установлено, что при введении органического поверхностно-активного вещества в электролит на границе катод - электролит дополнительное электрическое поле, связанное с адсорбцией органических молекул, не возникает. Это дало возможность на основании поляризационных кривых количественно определить величины как активных, так и пассивных участков катода. [34]
Таким образом, для количественного истолкования кривых дифференциальной емкости в присутствии органического вещества необходимо знать зависимости q q ( Е, 9) и0 9 ( Е), связанные с помощью уравнения ( 8) с изотермой адсорбции органических молекул на поверхности электрода. [35]
Молекулы органического вещества, как правило, адсорбируются лишь вблизи потенциала нулевого заряда, когда напряженность поля в двойном электрическом слое не слишком велика. Адсорбция органических молекул уменьшает диэлектрическую постоянную двойного электрического слоя и как бы раздвигает его обкладки. [36]
В первом приближении кривые дифференциальной емкости на твердых электродах в присутствии органических соединений аналогичны соответствующим кривым на жидкой ртути. При адсорбции органических молекул, которая имеет место при не слишком больших зарядах поверхности, наблюдается снижение емкости по сравнению с емкостью в чистом растворе фона, а при увеличении заряда электрода имеет место десорбция органического вещества, сопровождающаяся характерным пиком на кривых дифференциальной емкости. Пики на С, - кривых в случае твердых электродов выражены хуже, чем в случае жидкой ртути ( см. рис. 30), что, возможно, связано с неоднородностью твердой поверхности. [37]
При адсорбции на поверхности электрода ионов емкость двойного слоя возрастает вследствие уменьшения расстояния между обкладками конденсатора - поверхностью электрода и центрами адсорбированных ионов. При адсорбции незаряженных органических молекул из водных или водно-органических растворов емкость двойного слоя, наоборот, уменьшается из-за раз-движения обкладок конденсатора адсорбированным веществом и снижения диэлектрической постоянной между ними. [38]
При адсорбции заряженных частиц ( ионов) принимают во внимание сдвиг т.н.з. и изменение гргпотенциала, вызывающие повышение или понижение скорости электродного процесса. При адсорбции поверхностно-активных органических молекул образование адсорбционной пленки может влиять на стадию переноса электрона или на сопутствующие химические реакции. Стерические препятствия затрудняют нормальное протекание электродного процесса, а образование ионных пар, напротив, способствует увеличению его скорости. [39]
При адсорбции заряженных частиц ( ионов) принимают во внимание сдвиг т.н.з. и изменение - потенциала, вызывающие повышение или понижение скорости электродного процесса. При адсорбции поверхностно-активных органических молекул образование адсорбционной пленки может влиять на стадию переноса электрона или на сопутствующие химические реакции. Стерические препятствия затрудняют нормальное протекание электродного процесса, а образование ионных пар, напротив, способствует увеличению его скорости. [40]
Наряду со способностью адсорбировать полярные неорганические вещества глинистые минералы способны к адсорбированию полярных органических соединений. Наиболее изучена адсорбция органических молекул на монтмориллоните. [41]
Нами была изучена адсорбция акцепторных органических молекул хинонов на поверхности окиси алюминия. Оказалось, что в определенных условиях почти все изученные нами хиноны от фторанила, одного из сильнейших акцепторов, до антрахинона, акцепторные свойства которого незначительны, содержат в спектрах ЭПР один и тот же широкий сигнал, состоящий из шести компонент равной интенсивности. Спектр резко отличается от спектров соответствующих семихинонов по величине полного расщепления ( - 50 э) и сверхтонкой структуре и не содержит расщепления от кольцевых атомов водорода и фтора. [42]
Эти представления позже были конкретизированы Н. Д. Зелинским применительно к катализу реакций органической химии. Он указывал, что при адсорбции органической молекулы входящие в ее состав атомы углерода закрепляются па поверхности катализатора на соседних узлах кристаллической решетки. Поскольку расстояния между такими узлами не совпадают с расстояниями между атомами углерода в адсорбированной молекуле, последняя деформируется и связи внутри нее ослабляются. [43]
Способность электрода адсорбировать органические молекулы понижается при наличии скачка потенциала в двойном ионном слое. Наличие электрического поля ионного слоя затрудняет адсорбцию органических молекул. По мнению Фрумкина, это связано с тем, что поле втягивает в себя молекулы воды, имеющие большую диэлектрическую постоянную, вытесняя с поверхности органические молекулы. Очевидно, введением в электролит поверхностно-активных ионов, изменяющих знак и величину ионного слоя, можно изменить адсорбционную способность электрода. Некоторые конкретные примеры были рассмотрены выше. [44]
 |
Скорость пассивировани. цинково - [ IMAGE ] Скорость пассивирова. [45] |
Страницы: 1 2 3 4