Адсорбция - нейтральная молекула
Cтраница 1
Адсорбция нейтральных молекул, например амилового спирта, происходит в области потенциалов вблизи потенциала нулевого заряда. При потенциалах, удаленных от потенциала нулевого заряда, когда заряд электрода становится достаточно большим, к электроду электростатическими силами притягиваются полярные молекулы воды, вытесняющие с поверхности раздела электрод - раствор нейтральные молекулы органического вещества. [1]
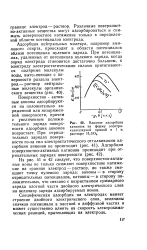 |
Влияние адсорбции катионов на форму электрокапиллярной кривой в 1 н. растворе H2SO4. [2] |
Адсорбция нейтральных молекул, например амилового спирта, происходит в области потенциалов вблизи потенциала нулевого заряда. [3]
Кроме адсорбции нейтральных молекул, часто наблюдается адсорбция ионов, содержащихся в растворе. Это процесс более сложный, чем молекулярная адсорбция. В большинстве случаев ионная адсорбция протекает необратимо и с повышением температуры часто возрастает. Следовательно, при адсорбции ионов твердыми поверхностями действуют не только силы молекулярного притяжения, но и химические силы. Адсорбция ионов имеет ярко выраженный избирательный характер. [4]
Помимо адсорбции нейтральных молекул часто наблюдается адсорбция ионов, содержащихся в растворе. Это процесс более сложный по сравнению с молекулярной адсорбцией. Рассмотрим водные растворы, имеющие наибольшее практическое значение. Адсорбция ионов в значительной степени зависит от природы адсорбента. Ионы, способные поляризоваться, адсорбируются, как правило, поверхностью веществ, состоящих из полярных молекул или ионов. Микроучастки поверхности, имеющие тот или иной заряд, адсорбируют только противоположно заряженные ионы. Противоионы электролита не адсорбируются поверхностью адсорбента, а накопляются вблизи ее, образуя двойной электрический слой. [5]
Наряду с адсорбцией нейтральных молекул адсорбируются ионы того или иного знака. Обычно адсорбируются те ионы, которые уже имеются в кристаллической решетке адсорбента, например А1 ( ОН) 3 легко адсорбирует ионы АГ и полярные молекулы воды. [6]
Такого рода стабилизация, достигаемая адсорбцией нейтральных молекул, происходит еще более наглядно в том случае, если адсорбированное вещество обладает свойствами коллоида. Причина такого явления не совсем ясна, но возможно, что оно частично имеет место под влиянием факторов геометрического характера, а частично находится в зависимости от фактора времени. Не исключена возможность, что в течение проверенных на практике промежутков времени может произойти адсорбция большего количества коллоидного вещества, чем это досягаемо путем индивидуальной адсорбции отдельных молекул. Во всяком случае описываемое явление настолько явно выражено, что это обстоятельство привело к созданию специального термина защитный коллоид. Свойства таких коллоидов присущи декстрину, смолам, белкам и др. веществом. В равной мере эффективными являются в данном отношении мыла и иные моющие средства. [7]
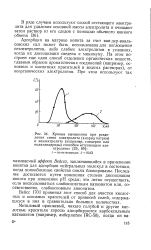 |
Кривые вымывания при разделении смеси электролита ( хлорид натрия и неэлектролита ( например, глицерин или полиглицериды способом отстающего электролита. / - полиглицернды. 2 - NaCl. [8] |
Вейсса, заключающийся в применении ионитов для адсорбции нейтральных молекул в состоянии, когда ионообменные свойства смолы блокированы. Последнее достигается путем изменения степени диссоциации ионита при изменении рН среды; это легко осуществить, если воспользоваться слабокислотным катионитом или, соответственно, слабоосновным анионитом. [9]
Аналогичное предположение сделал Фрумкин [4] при рассмотрении адсорбции нейтральных молекул при постоянной разности потенциалов на границе металл - раствор. Если характер изменения потенциала с расстоянием от электрода не зависит от заполнения поверхности, то потенциал в плоскости локализации адсорбированных частиц также остается постоянным. Так называемый эффект дискретности зарядов делает это условие малообоснованным в общем случае, хотя оно может быть более или менее правильным для нейтральных молекул. [10]
Поскольку имеет место перенос заряда, поверхностная концентрация адсорбированных частиц зависит от их электрохимического потенциала [ г в большей степени, нежели от химического потенциала ( л, определяющего величину адсорбции нейтральных молекул на поверхности, контактирующей с газовой фазой. [11]
Из полученных данных следует, что на поверхности твердого тела сохраняются такие характерные черты строения двойного слоя на ртути, как зависимость степени диффузности от концентрации, специфическая адсорбция анионов, влияние поля двойного слоя на адсорбцию нейтральных молекул. [12]
Обычно считают, что адсорбция веществ на электродах происходит только в определенном интервале потенциалов, зависящем от точки нулевого заряда: анионы адсорбируются преимущественно на положительно заряженной поверхности, катионы - на отрицательно заряженной поверхности, а нейтральные органические молекулы - вблизи потенциала нулевого заряда. Адсорбция нейтральных молекул и органических ионов на поверхности с большим зарядом невозможна. [13]
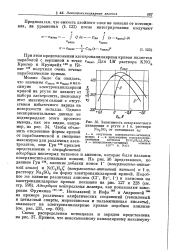 |
Зависимость поверхностного. [14] |
Подобное же влияние различных анионов ( С1 -, Вг -, I) и катионов на электрокапиллярные кривые показано на рис. 227 и 228 ( см. стр. Адсорбция нейтральных молекул, как показывают измерения Фрумкина 14014Й, Николаевой и Иофа 147 и Андреевой 148 на примере различных алифатических соединений ( гексиловый. [15]
Страницы: 1 2 3