Возможность - образование - водородная связь
Cтраница 1
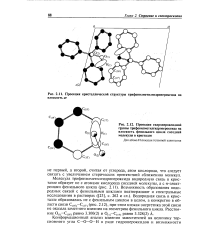 |
Проекция гидропероксидной группы трифенилметилгидропероксида на плоскость фенильного цикла соседней молекулы в кристалле. [1] |
Возможность образования водородных связей с фенильными циклами подтверждают и спектральные исследования в растворах ( [23], с. [2]
 |
Црс - и транс-формы молекулы орто-хлорфенола. [3] |
Возможность образования водородной связи отражается на физических свойствах хлорфенолов. Например, точка кипения о-хлорфенола равна 176 С, тогда как для мета и пара-изомеров она значительно выше. Это объясняется тем, что у двух последних изомеров межмолекулярная водородная связь играет более важную роль, чем в орто-изо-мере. [4]
Возможность образования водородной связи является результатом особых свойств атома водорода, а именно - наличия у него одного единственного электрона. Если облако отрицательного заряда электрона сильно смещается к другому атому ( что происходит, когда водород соединен ковалентной связью с сильно электроотрицательным элементом), то остается мало закрытый электронным облаком протон - частица с единичным зарядом и очень малым радиусом. Это создает возможность для дрнорно-акцепторного взаимодействия между протоном и неподеленной электронной парой сильно электроотрицательных элементов, таких как фтор, кислород, азот, входящих в состав другой молекулы. [5]
Возможность образования водородной связи в рассматриваемых молекулах определяется разностью электроотрицательностеи атомов в связях С - Н, N - Н, О - Н, Н - F. Фтор имеет самую высокую электроотрицательность. [6]
Возможность образования водородной связи отражается также и на физических свойствах хлор-фенолов. Например, точка кипения о-хлорфенола равна 176 С, тогда как для мета - и ара-изомеров она значительно выше. Это объясняется тем, что у двух последних изомеров межмолекулярная водородная связь играет более важную роль, чем в орто-изомере. [7]
Возможность образования водородной связи является результатом особых свойств атома водорода, а именно - наличия у него одного единственного электрона. Если облако отрицательного заряда электрона сильно смещается к другому атому ( что происходит, когда водород соединен ковалентной связью с сильно электроотрицательным элементом), то остается мало закрытый электронным облаком протон - частица с единичным зарядом и очень малым радиусом. Это создает возможность для дрнорно-акцепторного взаимодействия между протоном и неподеленной электронной парой сильно электроотрицательных элементов, таких как фтор, кислород, азот, входящих в состав другой молекулы. [8]
Возможность образования водородной связи отражается также и на физических свойствах хлор-фенолов. Например, точка кипения о-хлорфенола равна 176 С, тогда как для мета - и пара-изомеров она значительно выше. Это объясняется тем, что у двух последних изомеров межмолекулярная водородная связь играет более важную роль, чем в орто-изомере. [9]
Возможность образования водородной связи в рассматриваемых молекулах определяется разностью электроотрицательностеи атомов в связях С - Н, N - Н, О - Н, Н - F. Фтор имеет самую высокую электроотрицательность. [10]
Возможность образования водородной связи отражается также и на физических свойствах хлор-фенолов. Например, точка кипения о-хлорфенола равна 176 С, тогда как для мета - и пара-изомеров она значительно выше. Это объясняется тем, что у двух последних изомеров межмолекулярная водородная связь играет более важную роль, чем в орто-изомере. [11]
Возможностью образования водородных связей между макромолекулами целлюлозы объясняется ее прочность и способность к образованию волокон, а также неплавкость и трудная растворимость, несмотря на большое количество гидроксильных групп. [12]
Возможностью образования водородных связей между макромолекулами целлюлозы объясняется ее прочность и способность к образованию волокон, а также неплавкость и трудная растворимость, несмотря на большое количество гидроксильных групп. [13]
Сама возможность образования водородной связи определяется наличием протон-донорных групп у лиганда и протон-акцепторных центров у комплексного соединения в целом. Помимо этих условий для образования водородной связи необходимы благоприятные пространственные условия. [14]
Сама возможность образования водородной связи определяется наличием протонгдонорных групп у лиганда и протон-акцепторных центров у комплексного соединения в целом. Кроме этого, необходимы благоприятные пространственные условия. [15]
Страницы: 1 2 3 4