Изучение - белок
Cтраница 1
Изучение белков, меченых 57Fe, посредством этого метода показало, что подвижность их составных частей отлична от подвижности молекул в обычных кристаллах и жидкостях. Конформациопная подвижность в белках сохраняется и при низких температурах. [1]
Изучение белков навело на мысль, что между геном и конечным продуктом - ферментом - существуют промежуточные продукты, которые, однажды возникнув, могут в дальнейшем воспроизводить самое себя, по крайней мере в течение некоторого времени после того, как вызвавший их образование ген удален. В отдельных случаях проверка показала, что либо эти доказательства не слишком достоверны, либо предполагаемые плазмагены - всего лишь чужеродные вирусные частицы или что-нибудь в этом роде. Однако в других случаях все же удалось весьма убедительно показать, что плазмагенопо-добные тельца, по-видимому, действительно существуют. Один из наиболее известных плазмагенов найден у парамеции. В этом крошечном одноклеточном организме вырабатываются вещества, которые можно обнаружить благодаря тому, что, будучи введены кроликам, они вызывают в их крови образование специфических антител. Образование каждого вещества контролируется соответствующим плазмагеном. Плазмагены в свою очередь находятся под контролем генов, присутствующих в ядре, а на само ядро влияет цитоплазма клетки. Изменить состояние цитоплазмы можно, выращивая животных при различных температурах или изменяя внешние условия другим способом. То или иное состояние цитоплазмы вызывает к деятельности тот или иной ген; ген стимулирует образование соответствующего плазмагена; а этот последний в свою очеоедь индуцирует образование определенного конечного продукта. [2]
При изучении субъединичных белков и нуклеопротеидов аффинная модификация дает возможность понять, какие субъединицы участвуют в узнавании специфических лигандов. [3]
При осмотическом изучении белков, находящихся вдали от их изоэлектрической точки, необходимо, согласно уравнению ( 37), прибавлять достаточное количество электролита для понижения доннановского равновесия. XVIII будет показано, каким образом можно применить доннановское равновесие для объяснения набухания гелей белка, когда гель смещается со своей изоэлектрической точки. Набухание происходит вследствие увеличения осмотического давления внутри геля. Разность осмотических давлений всегда оказывается меньше, чем вычисленная. Этот эффект, впервые описанный Гаммарстеном, известен как эффект Гаммарстена. Он полагал, что присутствие большого коллоидного иона определенным образом понижает коэ-фициент активности малых ионов. Этот эффект исследовался многими другими авторами, но его причина осталась невыясненной. [4]
При изучении белков семян злаков мы видели, что в этих семенах содержание растворимых в спирте проламинов и извлекаемых щелочью глютелинов значительно превышает количество альбуминов и глобулинов. Изучение белкового комплекса семян бобовых культур показало, что в нем преобладают глобулины. В семенах гороха на долю глобулинов приходится свыше 60 % общего содержания белков, в семенах сои, люпина и чечевицы 60 - 70 %, в семенах фасоли 80 - 90 % общего содержания белков. [5]
Если сравнить изучение белка со штурмом крепости, можно сказать, что после длительной осады крепостные стены взяты и войска ученых остановились перед решающим штурмом внутренней, последней цитадели. Природа ревниво оберегает свои тайны, но ученые все время изобретают новое и новое оружие для атак. И каждый день приносит успехи. Что же сейчас сделано в этом направлении. Войдем за крепостные стены и осмотрим город, раскинувшийся перед нами. [6]
Учитывая при изучении белков трудности методического характера, а также ограниченную устойчивость этих соединений в рамках геологического времени, более рационально производить исследования аминокислот. Исследовать аминокислоты целесообразно по двум причинам. [7]
Очень часто при изучении белков не ограничиваются определением лишь общего содержания азота в каждой белковой фракции, а получают препараты соответствующих белков и затем используют их для определения аминокислотного состава. [8]
Основные научные работы посвящены изучению белков и биохимических окислительных процессов. [9]
К серьезным затруднениям при изучении белков приводит их большая склонность к определенным изменениям, называемым денатурацией. Почти все белки ( исключением является желатин) чувствительны к нагреванию; температурный коэффициент реакции весьма высок. [10]
К серьезным затруднениям при изучении белков приводит их большая склонность к определенным изменениям, называемым денатурацией. Почти все белки ( исключением является желатин) чувствительны к нагреванию; температурный коэффициент реакции весьма высок. Аналогичные изменения наступают при действии кислот, щелочей, спиртов, ацетона, мочевины, йодистого калия, трихлоруксусной, вольфрамовой и сульфосалициловой кислот, ультрафиолетового и рентгеновского облучений, при встряхивании или под действием высокого давления. Результат этих воздействий, если и неполностью одинаков, то имеет один и тот же характер. [11]
Однако с определения аминокислотного состава изучение белка только начинается. Можно подсчитать, что сравнительно простой белок, построенный из 20 остатков разных аминокислот, может за счет различного порядка их чередования иметь 2 - 1018 изомеров. [12]
Особое значение методов иммунодиффузии в изучении белков состоит в том, что с их помощью можно характеризовать белки на основании свойств, отличных от тех, которые были известны ранее. Электрофорез позволяет фракционировать белки в соответствии с их физико-химическими свойствами, в то время как с помощью классических методов иммунологии можно проводить дальнейшую дифференцировку белковых компонентов по антигенным свойствам. [13]
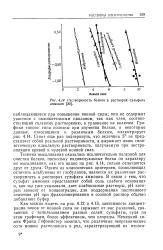 |
Растворимость белков в растворах сульфата аммония. [14] |
Графики такого типа полезны при изучении белков, и некоторые данные, относящиеся к различным белкам, иллюстрирует рис. 4.14. Стоит еще раз подчеркнуть, что величина S не представляет собой реальной растворимости, а выражает лишь гипотетическую идеальную растворимость, получаемую при экстраполяции кривой к нулевой ионной силе. [15]
Страницы: 1 2 3 4