Термодинамическая возможность
Cтраница 1
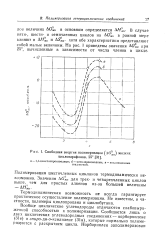 |
Свободная энергия полимеризации ( ДО К жидких циклопарафинов, 25. [1] |
Термодинамическая возможность не всегда гарантирует практическое осуществление полимеризации. Не известны, в частности, полимеры циклопропана и циклобутана. [2]
Термодинамическая возможность коррозии является условием обязательным, но недостаточным для определения скорости коррозии, так как фактические скорости электрохимических реакций зависят еще и от кинетических условий их протекания. Важным фактором является физическая и физико-химическая неоднородность границы раздела металл-электролит и прилегающих областей, приводящая к неоднородному ( гетерогенному) распределению на поверхности металла анодных и катодных реакций с образованием областей преимущественного развития анодной или катодной реакций. Эти области могут быть разделены и в течение коррозионного процесса перемещаться на поверхности металла, хотя в принципе возможно и совмещение этих реакций на одной площади. [3]
Термодинамическая возможность полимеризации циклов, так же как и положение равновесия, достигаемое в процессе превращения циклов и линейных полимеров, определяется изменением изобарно-изотермического потенциала при протекании этой реакции. [4]
Термодинамическая возможность полимеризации циклов, так же как и положение равновесия, достигаемое в процессе превращения циклов и линейных полимеров, определяется изменением свободной энергии при протекании этой реакции. [5]
Термодинамическая возможность образования кокса в результате глубокой полимеризации непредельных соединений обычно рассматривается по следующей схеме: олефины переходят в диоле-фины, которые затем полимеризуются. Оба процесса проходят на катализаторе и приводят к постепенному отложению кокса на его поверхности. [6]
Термодинамическая возможность взаимодействия карбидов с азотом уменьшается при переходе от карбидов металлов IV группы к карбидам металлов VI группы. В соответствии с этим увеличивается также температура начала их взаимодействия. [7]
Термодинамическая возможность полимеризации циклов, так же как и положение равновесия, достигаемое в процессе превращения циклов и линейных полимеров, определяется изменением изобарно-изотермического потенциала при протекании этой реакции. [8]
Термодинамическая возможность осуществления процесса, как известно, определяется значением изобарно-изотермического потенциала. Чем более отрицателен этот потенциал, тем термодинамически более вероятен процесс. [9]
 |
Зависимость от температуры Т энергии Гиббса ДС реакции конверсии метана ( / и реагирующей смеси в конверторе метана с начальным соотношением партаз ( 2, 2. 1 ( 3 и 4. 1 ( 4. [10] |
Термодинамическая возможность протекания реакции не означает, что она обязательно должна протекать. Это зависит от скорости реакции. Но условия, определяющие принципиальную невозможность ее протекания, гарантируют, что реакция протекать не будет. [11]
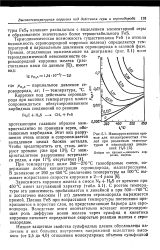 |
Изокоррозионные кривые для низкохромистых сталей при различных темпера. [12] |
Термодинамическая возможность существования FeS ( а отсюда возможность сероводородной коррозии железа) определяется температурой и парциальным давлением сероводорода в газовой фазе. [13]
Термодинамическая возможность полимеризации неорганических циклов, обрамленных органическими группами, а также положение равновесия, достигаемое в процессе превращения циклов в линейные полимеры, определяется изменением свободной энергии при реакции. Если запас свободной энергии звена неорганического цикла больше запаса свободной энергии элементарного звена полимерной молекулы, то реакция превращения цикла в полимер возможна. В этом случае процесс протекает с уменьшением свободной энергии, что обеспечивает большую термодинамическую устойчивость полимера по сравнению с циклом в условиях реакции. [14]
Термодинамическая возможность самопроизвольного протекания химической реакции определяется знаком и абсолютной величиной изменения энергии Гиббса ДОг или энергии Гельмгольца & FT в процессе химической реакции ( изменением изобарно-изотермиче-ского или изохорно-изотермического потенциала), найденной при постоянной температуре. [15]
Страницы: 1 2 3 4