Специфическая адсорбция
Cтраница 1
Специфическая адсорбция вызывает изменение ф2 - потен-циала. С помощью уравнения ( 2) легко установить, как должна измениться в результате этого скорость электродного процесса. Например, скорость восстановления анионов, адсорбирующихся лишь электростатически, при заданном потенциале уменьшается в присутствии анионов, адсорбирующихся специфически, и растет при добавлении специфически адсорбирующихся катионов. Противоположный вывод справедлив для восстановления катионов, адсорбирующихся лишь электростатически. Когда потенциал сдвигается к области десорбции, значения ф2 в растворах, содержащих и не содержащих поверх-ностноактивный электролит, сближаются между собой; поэтому тафелевские зависимости, полученные в растворе поверхностно-активного электролита, искажаются при этих потенциалах. Такой эффект обнаруживается на рис. 102; при построении этого графика не принималась в расчет блокировка поверхности электрода специфически адсорбированными анионами. [1]
Специфическая адсорбция в уравнениях ( 3) и ( 4) не учитывается. Вторые экспоненциальные члены соответствуют предположению о наличии линейной связи между свободной энергией активации прямого процесса и соответствующим изменением свободной энергии полного процесса. Это приводит к такому определению коэффициента переноса а, когда величину anF / v можно считать коэффициентом пропорциональности между изменением свободной энергии активации прямого процесса и падением потенциала на границе раздела фаз ( Pm - q2) f где qm - потенциал металла относительно глубины раствора электролита. [2]
Специфическая адсорбция на оптически активных адсорбентах. Одним из наиболее общих методов разделения неионных комплексов является, по-видимому, использование селективной адсорбции. До сих пор обычно используются два адсорбента - кварц и крахмал. Ни в одном случае не было достигнуто полного разделения. [3]
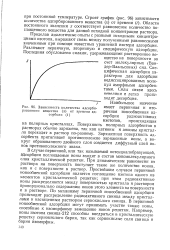 |
Зависимость количества адсорбированного вещества ( х от времени адсорбции ( t. [4] |
Специфическая адсорбция характерна для адсорбции недиссоциированных молекул аморфными адсорбентами. Силы связи здесь невелики и легко происходит десорбция. [5]
Специфическая адсорбция обусловлена притяжением частиц из раствора к поверхности ртути силами, по своей природе не являющимися чисто кулоновскими. Очень часто анионы специфически адсорбируются, а катиону - нет. В этом случае величину Г, которую можно получить термодинамически, непосредственно связывают с поверхностной концентрацией катионов в диффузной части двойного слоя. Тогда для рассмотрения диффузной части двойного слоя можно использовать теорию, изложенную в разд. [6]
Специфическая адсорбция ( или адсорбция потенциалопреде-ляющих ионов) наблюдается тогда, когда твердая поверхность избирательно поглощает ионы только одного вида, которые сообщают ей свой заряд. Это становится возможным, когда микроучастки поверхности, несущие определенный заряд, адсорбируют противоположно заряженные ионы. [7]
Специфическая адсорбция зависит от сролства адсорбируемых ионов к поверхности, их способности образовывать недиссоциирующие поверхностные соединения. Например, на кристаллах хорошо адсорбируются из раствора ионы, образующие с ионами кристалла нерастворимые соединения. Большими адсорбционными потенциалами обладают многозарядные ионы ( А. [8]
 |
Прибор для наблюдения электроосмоса. [9] |
Специфическая адсорбция может вызвать и уменьшение - потенциала, если адсорбируются противоионы, так как они имеют заряд, противоположный заряду поверхности. [10]
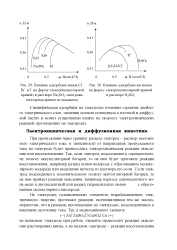 |
Влияние адсорбции ионов С1, [ IMAGE ] Влияние адсорбции катионов. [11] |
Специфическая адсорбция на электродах изменяет строение двойного электрического слоя, значения скачков потенциала в плотной и диффузной частях и может существенно влиять на скорость электрохимических реакций, протекающих на электродах. [12]
Специфическая адсорбция обусловлена притяжением частиц из раствора к поверхности ртути силами, по своей природе не являющимися чисто кулоновскими. Очень часто анионы специфически адсорбируются, а катионы - нет. В этом случае величину Г, которую можно получить термодинамически, непосредственно связывают с поверхностной концентрацией катионов в диффузной части двойного слоя. Тогда для рассмотрения диффузной части двойного слоя можно использовать теорию, изложенную в разд. [13]
Специфическая адсорбция - промежуточная форма, когда некулоновск силы взаимодействия превалируют над электростатическими силами отталкива ния ( например, адсорбция анионов на одноименно заряженной поверхности) По Л. И. Антропову [8, 17], силы специфической адсорбции имеют электриче скую природу. [14]
Специфическая адсорбция определяется в значительной степени свойствам. Так, например специфическая адсорбция ионов галоидов наблюдается для большинства метал лов, многие ингибиторы, содержащие в молекуле я-связи, неподеленную пар; электронов, также адсорбируются специфически. [15]
Страницы: 1 2 3 4