Специфическая адсорбция - катион
Cтраница 2
Это предположение полностью подтверждается экспериментально обнаруженным фактом практического отсутствия специфической адсорбции катионов даже при отрицательном заряде электрода. Таким образом, при положительном заряде электрода адсорбция катионов должна быть еще более слабой. [16]
Ниже будут рассмотрены некоторые закономерности, возникающие, во-первых, при специфической адсорбции катионов и анионов, а также полярных молекул и, во-вторых, - при специфической адсорбции органических молекул с длинной углеводородной цепью. [17]
Этот вывод находит подтверждение в работах А. Н. Фрумхина и сотрудников в области специфической адсорбции катионов на положительно заряженной поверхности. [18]
Для непроводящей твердой фазы ( в отличие от металлов и полупроводников) одновременная специфическая адсорбция катионов и анионов наблюдается весьма редко; поэтому одним из слагаемых правой части обычно пренебрегают. [19]
Этот важный результат позволяет исключить гипотезу совместной адсорбции как единственное объяснение анионного эффекта ( гипотеза состоит в допущении, что специфическая адсорбция катиона таким образом видоизменяет распределение потенциала в двойном слое, что специфическая адсорбция поверхностно-активных анионов оказывается увеличенной вследствие возрастания их концентрации в диффузной части двойного слоя; этот эффект проявляется тем сильнее, чем более поверхностно-активным является анион, так как специфическая адсорбция аниона способствует в свою очередь адсорбции дополнительного количества катионов. [20]
Это явление можно объяснить на основании уравнения (52.2) теории замедленного разряда, если учесть, что z0 - 0, а при специфической адсорбции катионов ipi - потенциал сдвигается в положительную сторону. В отсутствие органических катионов скорость электровосстановления анионов мала, и их концентрация у поверхности близка к объемной. [21]
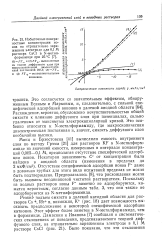 |
Избыточные поверхностные концентрации ионов на отрицательно заряженном электроде для 0 1 М раствора CsCl в N-метил-формамиде при 25 С. [22] |
Резкий додъем емкости в далекой катодной области для растворов Cs, Rb и, возможно, К ( рис. 18) дает возможность высказать предположение о некоторой специфической адсорбции катионов. Этот эффект более заметен в N-метилформамиде, чем в формамиде. [23]
Если предположить, что адсорбция происходит только за счет электростатического взаимодействия катионов ингибитора с отрицательно заряженной поверхностью металла через слой молекулярного сероводорода, то поскольку слой сероводорода может только ослабить это взаимодействие, эффективность защиты в этом случае должна была бы несколько снизиться, Следует допустить поэтому наличие специфической адсорбции катионов ингибитора на поверхностном слое сероводорода. Адсорбируясь на слое сероводорода, катионоактивный ингибитор создает энергетический барьер за счет ф - - потенциала, который препятствует подводу ионов гидроксония. Ингибитор таким образом блокирует молекулы сероводорода, уменьшая образование ионов сульфония. [24]
Кроме того, возможны реакции изомеризации. Специфическая адсорбция катионов приводит к изменению соотношения скоростей этих реакций. В то же время подавляется изомеризация непредельных соединений. В этой связи следует остановиться на свойствах родиевого катализатора. Ранее Биком при гидрировании этилена в газовой фазе на пленках и нами при гидрировании коричной кислоты в спиртовых растворах на никелевых катализаторах на силикагеле, промотиро-ванных металлами VIII группы, было показано, что Rh является наиболее активным катализатором. Однако в дальнейшем оказалось, что при гидрировании других непредельных соединений ( производные ацетилена и др.) родий оказался менее активным, чем никель, платина и особенно палладий. При гидрировании на различных катализаторах лимитирующие стадии иногда меняются, а сравнение активностей правомерно в пределах одного механизма. [25]
Мотт, Парсонс и Уоттс-Тобин [54] объяснили данный эффект исходя из предположения, что диэлектрическая проницаемость воды возрастает очень быстро с расстоянием от электрода и поэтому размеры катиона не играют существенной роли. Специфическая адсорбция катиона должна учитываться при более детальном рассмотрении, чем то, которое было развито этими авторами. [26]
По мере дальнейшего понижения содержания воды образуется в значительных количествах олигомер и выход адиподинитрила уменьшается. Благодаря высокой специфической адсорбции катионов четвертичных солей аммония последние, адсорбируясь на поверхности электрода, вытесняют молекулы воды из двойного электрического слоя. Образуется своего рода органический слой, обладающий низкой протоно-донорной способностью. [27]
 |
Спектр размеров частиц и пор фильтров. [28] |
Так, специфическая адсорбция катионов, например Mg2, Са2, катионов тяжелых металлов и Н, и анионов, па-пример SO42 -, HP042 -, SiO ( OH) 3 - и ОН -, на поверхности гидр-оксидов Si, Al3 или Fe3 обусловлена зарядом этих частиц. [29]
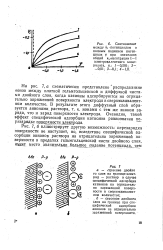 |
Соотношение между h - потенциалом и полным падением потенциала 9 при значениях общей концентрации I - I. [30] |
Страницы: 1 2 3 4