Быстрая адсорбция
Cтраница 2
При смачивании породы водой и поверхностно-активными веществами ( ПАВ) за счет смачивания поверхности или быстрой адсорбции ПАВ на вновь образованных поверхностях трещин выкола экранируются силы взаимодействия между берегами трещин, создается препятствие смыканию трещин. Это повышает эффективность разрушения, особенно в усталостной области разрушения, когда единичного удара недостаточно для выкола. Расклинивающее действие воды, ПАВ наиболее заметно проявляется в пористых и высокопроницаемых породах. Зоны повышенной трещиноватости, предразруше-ния создаются резцом при неоднократных проходах по забою. Смачивание обусловливает скол породы при меньшем числе циклов нагружения или при меньших нагрузках. При повышении плотности породы скол происходит при меньших деформациях, соответственно меньше и нагрузка, и объем разрушенной породы, требуемое время на сколообразование также уменьшается. [16]
Наряду с развитием газовой хроматографии большое практическое значение приобрела капиллярная хроматография, в которой создаются условия для быстрой адсорбции, благодаря чему можно разделять очень сложные смеси в течение нескольких минут. [17]
Селвуд ( P. W. Selwood, Northwestern University): Медленное поглощс-ние водорода никелем, которое может наблюдаться после того, как процесс быстрой адсорбции закончен, вызывает только незначительные изменения намагничивания, наблюдаемые при комнатной температуре. Но изменения намагничивания, вызываемые таким образом, возрастают по величине, если намагничивание измеряется при низких температурах. Следовательно, медленное поглощение является истинной хемосорб-цией, происходящей на более мелких частицах никеля. Не имеется никаких новых данных относительно того, почему процесс протекает медленно, но мы думаем, что скорость этого процесса определяется диффузией в направлении к менее доступным частицам никеля. [18]
Одна из гипотез о механизме сорбции макромолекул ГМЦ на поверхности волокон целлюлозы [315, 481, 482, 680, 770] предполагает, что при соприкосновении с раствором ГМЦ начинается быстрая адсорбция цепей ГМЦ на открытой поверхности целлю-люзы, причем гибкие макромолекулы адсорбируются через сегменты или короткие последовательности цепей. Между адсорбированными сегментами существуют неадсорбированные участки, образующие мостики, или иетли, простирающиеся в раствор. В раствор могут простираться и неадсорбированные сегменты у концов цепей. Предполагается, что характер адсорбционных сил определяется образованием водородных свзей между доступными гидроксилами. После заполнения в основном свободной поверхности целлюлозы сорбированными цепями ГМЦ начинается более медленная стадия сорбции макромолекул ГМЦ на уже сорбированные ГМЦ. [19]
Исследования напыленных металлических пленок [60, 61] показывают, что для некоторых переходных металлов ( например, родия, вольфрама, молибдена, кобальта, никеля) быстрая адсорбция кислорода при 77 - 90 К и давлении около 10 2 Па ( - 10 - 4 мм рт. ст.) ограничена заполнением монослоя с Хт-2. Достаточно надежно можно считать, что другие благородные металлы VIII группы ведут себя аналогично. Однако поглощение кислорода на железе в этих условиях намного превышает емкость монослоя, так же ведет себя титан. [20]
На основании изучения кинетики гидролиза п-нитрофенил-ацетата [6] и 2 4-динитрофенилацетата [8] по методу остановленного потока мы можем различить три стадии в этих реакциях: первая - начальная быстрая адсорбция субстрата, вторая - освобождение одного моля нитрофенола на моль химотрипсина и сопутствующее ацилирование группы у фермента и третья - гидролиз соединения фермент-ацил. Стадия начальной адсорбции протекает слишком быстро и не поддается измерению имеющимися в настоящее время методами. Эти величины характеризуют химическую реакцию между группами на каталитическом центре и субстратом и могут быть использованы в отдельности. Как освобождение ионов нктрофенилата, так и освобождение или связывание ионов водорода протекает во время обеих последовательных реакций. Найдено, что во время первой из них освобождается только нитрофенол, тогда как ацетат реагирует с ОН-группой фермента. Полученное соединение ацил-фермент во время конечной стадии гидролизуется с освобождением ацетата. Как ацилирование, так и гидролиз ацил-фермента ингиби-руется путем присоединения протона к соседней основной группе, вероятно имидазольной. В литературе приведено большое число доказательств, 8 ] в пользу того, что ацилируется именно гидроксильная группа в остатке серина в химотрипсине. [21]
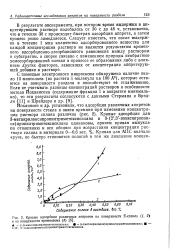 |
Кривые адсорбции различных аппретов на поверхности Е - стекла ( /, 2 и на поверхности кремнезема ( 3. [22] |
В результате эксперимента, при котором время выдержки в ал-претирующем растворе колебалось от 30 с до 48 ч, установлено, что в течение 30 с происходит быстрая адсорбция аппрета, а затем процесс резко замедляется. Следует отметить, что после выдержки в течение 1 мин количество адсорбированного вещества для; каждой концентрации раствора не является результатом временного адсорбционно-десорбционного равновесия между раствором: и субстратом, а скорее связано с изменением природы необратимо хемосорбированной пленки в ( процессе ее образования либо с влиянием других факторов, зависящих от концентрации аппретирующей добавки в растворе. [23]
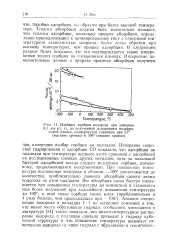 |
Изобары сорбции водорода при давлении 0 1 мм рт. ст. на полученной испарением вольфрамовой пленке, подвергнутой спеканию при 23 ( верхние кривые и 500 ( нижние кривые. [24] |
Измерение скоростей гидрирования и адсорбции СО показало, что адсорбция на палладии при температуре жидкого азота сравнима с адсорбцией на исследованных пленках других металлов, хотя за начальной быстрой адсорбцией всегда следует медленная сорбция, невидимому, продолжающаяся неограниченно. При повышении температуры поглощение водорода в области - 100 увеличивается до количества, приблизительно равного абсорбции одного атома водорода на атом палладия. [25]
Это может быть вызвано следующими причинами: 1) неравномерным смачиванием ткани, 2) недостаточной циркуляцией жидкости в ванне и вызванной этим неравномерностью концентрации раствора красителя, соприкасающегося с тканью, 3) слишком быстрой адсорбцией красителя на поверхности ткани, вероятно происходящей под действием сил электростатического притяжения; в этом случае в отличие от обычного, более медленного процесса крашения, когда краситель проникает внутрь волокна, возникают неравномерно окрашенные участки. [26]
Этот вывод был также получен при сопоставлении изобар для пленок металлов, испаренных в вакууме и при давлении азота 1 мм рт. ст. Найдено [1], что при давлении азота 1 мм, рт. ст. получаются ориентированные пленки, имеющие для быстрой адсорбции вдвое большую поверхность, чем поверхность неориентированных пленок такого же веса, полученных в высоком вакууме. На обоих типах пленок в небольшой степени идет и медленная сорбция. Однако позже было установлено, что в обоих этих случаях медленная сорбция одинакова, что также указывает скорее на весовой эффект, чем на связь с наличной поверхностью. Во-вторых [1], показано, что для ориентированных и не ориентированных пленок, спекавшихся при более высоких температурах, адсорбция окиси углерода при комнатной температуре уменьшалась пропорционально активности пленок обоих типов при гидрировании этилена. Опыты, подобные обсужденным в предыдущем разделе, показали, что измеренные методом БЭТ по вандерваальсовой адсорбции криптона при - 196 поверхности пленок, спекавшихся при различных температурах, также уменьшаются пропорционально уменьшению активности при гидрировании этилена при комнатной температуре. Таким образом, как относительная хемо-сорбция окиси углерода при комнатной температуре, так и ван-дерваальсова адсорбция криптона представляют надежные способы измерения поверхности, доступной для гидрирования этилена. Это же относится и к быстрой адсорбции водорода при - 196, так что она представляет третий критерий, при помощи которого можно определять каталитически активную поверхность подвергавшихся спеканию пленок. [27]
Эти опыты ясно показывают, что ранее наблюдавшаяся медленная адсорбция водорода на никелевых катализаторах представляет не адсорбцию, а сорбцию, состоящую из адсорбции и абсорбции водорода, причем последняя происходит в местах, не доступных для окиси углерода, криптона и быстрой адсорбции водорода при - 196 и не доступных также для этилена. [28]
Казалось, что два экспериментально установленных факта делали этот механизм трудно обосновываемым: а) хотя эта конверсия идет на вольфрамовой нити при - 110, Франкенбургер и Годлер [4] нашли, что адсорбция водорода на порошкообразном вольфраме ниже 150 очень мала, а б) Роберте [5] измерил теплоты адсорбции водорода на очень чистых вольфрамовых нитях и получил очень большие теплоты адсорбции при всех степенях заполнения поверхности ( см. рис. 37, кривая J), хотя при низких температурах и происходила очень быстрая адсорбция. [29]
Другие авторы связывают роль некоторых блескообразующих добавок со скоростью их адсорбции и десорбции на поверхности электрода. Быстрая адсорбция и десорбция молекул поверхностно-активного вещества препятствует осаждению металла в виде крупных кристаллов и способствует сглаживанию поверхности. [30]
Страницы: 1 2 3 4