Интерметаллическая фаза
Cтраница 1
Интерметаллические фазы стабильнее сверхструктур, они большей частью твердые, хрупкие и обладают плохой электропроводностью. [1]
Интерметаллические фазы не повторяют структурные типы компонентов, из которых они образованы. В них атомы разных сортов занимают определенные позиции в структурах. Этим фазам часто приписывают формулы, не отвечающие формальным валентностям и точному химическому составу. Промежуточное положение дает основание называть их интерметаллическими фазами. [2]
Интерметаллические фазы и соединения с частично полярным типом связи известны как цинтл-фазы. По данным рентгеноструктурного анализа, в этих соединениях радиус атомов менее активного металла имеет практически постоянную величину, в то время как радиус атома более активного металла значительно уменьшен. Атомы менее активного металла образуют основную решетку, в пустотах которой находятся атомы более активного металла. [3]
Интерметаллические фазы примыкают к настоящим химическим соединениям с определенным стехиометри-ческим составом. [4]
Интерметаллические фазы стабильнее сверхструктур, они большей частью твердые, хрупкие и обладают плохой электропроводностью. [5]
Обычно интерметаллические фазы не имеют постоянного стехиометрического состава. Их состав может меняться в определенных пределах без изменения структуры. Иногда удается наблюдать переход из состояния со статистическим распределением в упорядоченное состояние. Так, в кубической объемно-центрированной р-фазе CuZn атомы Си и Zn статистически распределены по позициям /, при отжиге этой фазы при низких температурах возникает сверхструктура типа CsCl ( рис. В. [6]
Неравновесные избыточные интерметаллические фазы образуются в электроосажденных вблизи предельного тока ( inp) сплавах, которые в равновесном состоянии однофазны. Как показали результаты рентгеноструктурного анализа и электронной микроскопии, отжиг при темперотурпх ( 0 4 - 0 5) Тпл сравнительно быстро приводит к растворению избыточных фаз и переходу атомов легирующих компонентов в твердый раствор. Однако по данным мессбауэровской спектроскопии даже после длительного отжига в сплавах сохраняется концентрационная неоднородность. [7]
Двухкомпонентную интерметаллическую фазу ( как и многокомпонентную), строго говоря, нельзя представить себе в виде простой двух-электродной системы. Энергетические состояния компонентов в сплаве, как уже отмечалось в теоретической части этой главы, могут значительно отличаться от энергетического состояния чистых компонентов. В то же время кинетические особенности поведения компонентов как в сплаве, так и в собственной фазе остаются без существенных изменений. [8]
 |
Теплота образования некоторых гидридов, ккал / моль Н2. [9] |
Подобно интерметаллическим фазам многие гидриды переходных металлов имеют переменный состав, изменяющийся в широком интервале концентраций. В связи с этим особенно часто возникает вопрос: чем является та или другая гидридная фаза, химическим соединением или раствором. [10]
Некоторые интерметаллические фазы используются для упрочнения аустенитных и ферритных жаропрочных, магнитных и других сплавов. Упрочнение достигается в результате закалки и старения, которые можно осуществить, если растворимость соединения в железе возрастает с повышением температуры. В обычных массовых сталях интерметаллнческие соединения не встречаются. [11]
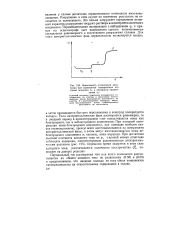 |
Зависимость потенциала электрода при переменной поляризации его током анодного та и катодного направления тк. [12] |
Если интерметаллическая фаза растворяется равномерно, то в анодный период в приэлектродном слое накапливаются ионы как благородного, так и неблагородного компонентов. При катодной поляризации ионы благородного компонента, как имеющие наиболее низкое перенапряжение, прежде всего восстанавливаются на поверхности интерметаллической фазы, а затем могут восстанавливаться иО ны неблагородного компонента и, наконец, ионы водорода. Определив время задержки и зная силу катодного тока, рассчитывается количество электричества QR, пошедшее на данную реакцию. [13]
Устойчивость интерметаллических фаз зависит от электронной структуры металлов и связана с электронной концентрацией el a - отношением числа валентных электронов к числу атомов в соединении или элементарной ячейке. По мере увеличения е / а и достижения определенного значения образуется новая фаза с другой структурой и устойчивая в данном интервале электронных концентраций. Юм Ро-зери установил, что такие фазы возникают при е / а 1 5, 1 62 и 1 75, что подтверждено на большом числе двойных систем. Для фаз Лавеса идеальнее отношение размеров атомов равно 1 225, а структура зависит от е / а. [14]
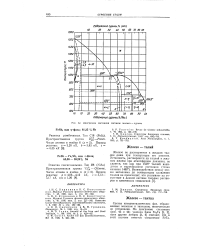 |
Диаграмма состояния системы железо - сурьма. [15] |
Страницы: 1 2 3 4 5