Интерметаллическая фаза
Cтраница 2
Состав интерметаллических фаз, образованных железом и танталом, окончательно не установлен. [16]
 |
Диаграмма состояния системы железо - тантал.| Диаграмма состояния системы железо - тантал. [17] |
Состав интерметаллических фаз, образованных железом и танталом, окончательно не установлен. На диаграмме состояния ( рис. 43 и 44) указана фаза Fe2Ta [1, 2], хотя другие авторы [3, 4] считают, что в системе Fe - Та имеется соединение FeTa. Возможно также существование нескольких других соединений. Не исключено, что сплавы, содержащие 50 - 70 % Та, испытывают превращения в твердом состоянии. Имеющийся экспериментальный материал совершенно недостаточен для полного объяснения этого участка диаграммы. [18]
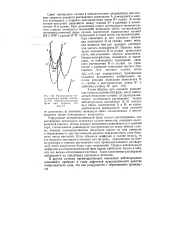 |
Расположение потенциальных кривых компонентов янтерметаллической фазы при условии, что. [19] |
Разрушение интерметаллической фазы нельзя рассматривать как растворение нескольких отдельных кусков металлов, имеющих электрический контакт. Атомы каждого компонента равномерно ( по крайней мере, статистически равномерно) распределены по всему объему сплава, поэтому преимущественная ионизация одного из них приводит к образованию в кристаллической решетке поверхностного слоя большого числа вакансий. Если объемная диффузия в сплаве велика, то эти вакансии занимаются атомами того же рода, пришедшими из объема раствора и процесс растворения ( или преимущественного растворения) этого компонента будет идти непрерывно. [20]
Разрушение интерметаллических фаз ( твердых растворов, интерметаллических соединений), как уже обсуждалось в теоретической части этой главы, может быть равномерным и селективным. [21]
Устойчивость интерметаллических фаз зависит от электронной структуры металлов и связана с электронной концентрацией el a - отношением числа валентных электронов к числу атомов в соединении или элементарной ячейке. По мере увеличения el а и достижения определенного значения образуется новая фаза с другой структурой и устойчивая в данном интервале электронных концентраций. Юм Ро-зери установил, что такие фазы возникают при е / а 1 5, 1 62 и 1 75, что подтверждено на большом числе двойных систем. Для фаз Лавеса идеальное отношение размеров атомов равно 1 225, а структура зависит от е / а. [22]
Индий образует интерметаллические фазы ( бертоллидного типа) с некоторыми близкими металлами, такими, как олово и свинец. Целый ряд фаз ( так называемых электронных соединений) образуется в системах с металлами подгруппы меди. Большим числом интерметаллических соединений характеризуются системы индия с магнием, никелем, редкоземельными металлами. [23]
Индий образует интерметаллические фазы ( бертоллидного типа) с некоторыми близкими металлами, в частности с оловом и свинцом. Целый ряд фаз ( так называемых электронных соединений) образуется в системах с металлами группы меди. Большим числом интерметаллических соединений характеризуются системы индия с магнием, никелем, редкоземельными металлами. [24]
Индий образует интерметаллические фазы ( бертоллидного типа) с некоторыми близкими металлами, такими, как олово и свинец. Целый ряд фаз ( так называемых электронных соединений) образуется в системах с металлами подгруппы меди. Большим числом интерметаллических соединений характеризуются системы индия с магнием, никелем, редкоземельными металлами. [25]
Специфика исследований интерметаллических фаз состоит в том, что недостаточно изучить их общие свойства, а необхо-ди мо установить свойства каждого компонента, которые, есте-ственно, отличны от свойств чистого компонента. Особенностью коррозионных испытаний твердых растворов и интерметаллических соединений является определение в продуктах коррозии доли каждого компонента изучаемого сплава. [26]
Характер разрушения интерметаллических фаз, прежде всего, определяется термодинамикой и кинетикой анодного процесса, поэтому основное внимание уделяется анодному поведению твердых растворов и янтерметаллических соединений. [27]
Анодное поведение интерметаллических фаз зависит от электрохимических и физических свойств компонентов. [28]
При погружении интерметаллической фазы в раствор электролита на границе фаза - раствор возникает гальваническая разность потенциалов и тогда приведенные кривые характеризуют уже изменение электрохимического потенциала. [29]
 |
Расположение потенциальных кривых компонентов при различных потенциалах интерметаллической фазы. Потенциальные кривые обозначены. [30] |
Страницы: 1 2 3 4 5