Возрастание - растворимость
Cтраница 1
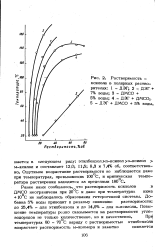 |
Растворимость - ксилола в полярных растворителях. 1 - ДЭГ. 2 - ДЭГ 7 % воды. 3 - ДМСО 5 % воды. 4 - ДЭГ ДМСО.. 5 - ДЭГ ДМСО 5 % воды. [1] |
Ощутимое возрастание растворимости не наблюдается даже при температурах, превышающих 100 С, и критическая температура растворения находится за пределами 180 С. [2]
 |
Ровновесие системы A12 ( S04 3 - A1F3 - H20 при 25. [3] |
Однако возрастание растворимости A1F3 ( раствор, насыщенный A1 ( NO3) 3 - 9H2O и A1FS - 3H2O, содержит 37 9 % А1 ( МО3) 3 и 5 38 % A1F3) показывает, что и в этом случае в растворе происходит образование комплексных соединений. [4]
Иногда такое возрастание растворимости может быть обусловлено и другими причинами, в частности явлениями гидролиза, возрастанием ионной силы раствора и уменьшением коэффициентов активности ионов малорастворимой соли. Так, К. Б. Яцимирским и А. А. Шутовым [28] показано, что растворимость PbJ2 увеличивается в растворах Ca ( NO3) 2 и Mg ( NO3) 2, хотя катионы кальция и магния мало склонны к образованию комплексных ионов и, с другой стороны, нитратокомплексы свинца либо не существуют, либо весьма непрочны. Поэтому, исследуя комплексные соединения, методом растворимости, обычно сохраняют постоянными ионную силу и рН раствора. [5]
Иногда такое возрастание растворимости может быть обусловлено и другими причинами, в частности явлениями гидролиза, возрастания ионной силы раствора и уменьшения коэффициентов активности ионов малорастворимой соли. Так, К. Б. Яцимирским и А. А. Шутовым [28] показано, что растворимость PbJ2 увеличивается в растворах Са ( МОз) г и Mg ( NO3) 2, хотя катионы кальция и магния мало склонны к образованию комплексных ионов и, с другой стороны, нитратокомплексы свинца либо не существуют, либо весьма непрочны. Поэтому, исследуя комплексные соединения методом растворимости, обычно сохраняют постоянными ионную силу и рН раствора. [6]
В порядке возрастания растворимости наиболее распространенные минералы располагаются в следующий ряд: силикаты и кремнезем - карбонаты - сульфаты - хлориды. Рост температуры, как правило, повышает растворимость большинства растворенных в ГПВ соединений. [7]
 |
Схема фазовых равновесий для систем, состоящих из ограниченно растворимых жидкостей ( случай II. [8] |
Рассмотрим случай возрастания растворимости с ростом температуры ( рис. 117), что обусловлено положительными значениями дифференциальных теп-лот растворения жидкостей. Кривая а / С выражает растворимость второй жидкости в первой; кривая ЬК - растворимость первой жидкости во второй. [9]
Растворители по возрастанию растворимости в них формиата натрия могут быть расположены в следующем порядке: этилаце-тат метилэтилкетон ацетон изобутиловый спирт к-ами-ловый спирт. [10]
Судя по величине возрастания растворимости, один моль NaF связывает в растворе 2 5 - 3 5 моля борной кислоты. Это, а также высокая вязкость раствора, дает основание полагать, что в растворе образуются фторозамещенные полибораты с цепочечными анионами. Сложный характер взаимодействия указывает, что эта система не должна рассматриваться как простая тройная система. [11]
Это выражение указывает на несколько большее возрастание растворимости, чем можно было бы ожидать при замене смеси разбавителя с мономером одним только разбавителем со значением х, соответствующим среднему значению для смеси мономер - разбавитель; для этой ситуации справедливо то же выражение, только без члена Xm. В обоих случаях общий результат состоит в значительном возрастании растворимости с увеличением концентрации мономера или хорошего растворителя, так как Xm. [12]
С увеличением содержания MgCl2 в растворе возрастание растворимости КС1 уменьшается. [13]
Из этих данных видно, что порядок возрастания растворимости подобен порядку возрастания основности, приведенной во второй графе. Здесь снова мезитилен является более сильным основанием, чем ксилолы. [14]
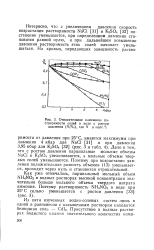 |
Относительное изменение растворимости солей в воде с ростом давления ( N / N0, где N в масс. %. [15] |
Страницы: 1 2 3 4