Вторичная обменная адсорбция
Cтраница 3
Наибольшее значение для радиохимии имеют лишь два вида адсорбции на гетерополярных адсорбентах - первичная обменная и вторичная обменная. В присутствии значительного избытка в растворе собственных ионов осадка главную роль обычно играет вторичная обменная адсорбция. [31]
Внутренняя адсорбция характеризуется резко выраженной зависимостью константы фракционирования от присутствующих в системе многовалентных ионов того же знака, что и адсорбируемый элемент. Это указывает на то, что по своей природе процессы внутренней адсорбции имеют много общего с процессами вторичной обменной адсорбции. [32]
Потенциалобразующая адсорбция ионов радиоактивных изотопов, находящихся в крайне разбавленном состоянии, играет незначительную роль, так как избыток ионов какого-либо знака в поверхностном слое кристалла против стехиометрического отношения может образоваться лишь в присутствии весомых количеств элемента. Вместе с тем Потенциалобразующая адсорбция косвенно имеет большое значение для адсорбции радиоактивных изотопов, так как ее величина определяет общую емкость по отношению к вторичной обменной адсорбции. [33]
Потенциалобразующая адсорбция ионов радиоактивных изотопов, находящихся в крайне разбавленном состоянии, играет незначительную роль, так как избыток ионов какого-либо знака в поверхностном слое кристалла против стехиомет-рического отношения может образоваться лишь в присутствии весомых количеств элемента. Вместе с тем потенциалобразую-щая адсорбция косвенно имеет большое значение для адсорбции радиоактивных изотопов, так как ее величина определяет общую емкость по отношению к вторичной обменной адсорбции. [34]
В качестве адсорбента следует, за весьма редкими исключениями, применять труднорастворимые и легко поддающиеся очистке кристаллические соединения. Малая растворимость вещества адсорбента приводит к удобному соотношению между количеством собственных ионов на его поверхности и в растворе, что особенно существенно при изучении первичной обменной адсорбции. При изучении вторичной обменной адсорбции это свойство адсорбента позволяет установить влияние конкурирующих ионов в широком интервале концентраций. Следует отметить также, что малая растворимость является одним из факторов, позволяющих свести до минимума скорость рекри-сталлизационных процессов, а следовательно, и изменение величины поверхности адсорбента во время опытов. [35]
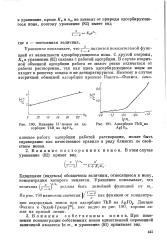 |
Влияние Н - ионов на адсорбцию ThB на AgJO3.| Адсорбция ТЬВ на AgJ03. [36] |
Уравнение показывает, что является показательной функцией от валентности адсорбирующегося иона. С другой стороны, К0 в уравнении ( 82) связана с работой адсорбции. В случае вторичной обменной адсорбции работа ее может резко отличаться от работы растворения, так как здесь адсорбирующиеся ионы не входят в решетку осадка и не дегидратируются. [37]
С другой стороны, Кй в уравнении ( 44) связана с работой адсорбции. В случае вторичной обменной адсорбции работа ее может резко отличаться от работы растворения, так как здесь адсорбирующиеся ионы не входят в решетку осадка и не дегидратируются. Поэтому в случае вторичной обменной адсорбции правило Панета-Фаянса, заменяющее работу адсорбции работой растворения, может быть справедливо как качественное правило в ряду близких по свойствам ионов. [38]
Между сульфидными и оксигидратными сорбентами существует и определенная аналогия. Роль акво -, ОН-групп и атомов кислорода могут выполнять в сульфидах соответственно H2S -, HS-группы и атомы серы. Эти группы участвуют в процессе взаимодействия ионов металлов с поверхностью сульфидов, что авторы работ [20-22] рассматривают как вторичную обменную адсорбцию. [39]
Процесс внутренней адсорбции характеризуется константой для данной концентрации, что внешне сближает его с образованием смешанных кристаллов. В отличие от последних внутренняя адсорбция уменьшается при увеличении концентрации распределяющего вещества. Сильная зависимость константы распределения от присутствия посторонних многовалентных ионов показывает, что этот процесс имеет много общего с вторичной обменной адсорбцией. [40]
В качестве примера можно привести исследования Курбатова с сотрудниками [ 15в ], посвященные изучению адсорбции двухвалентных радиоактивных изотопов Sr, Ba, Ra, Co на осадке гидрата окиси железа. Постановка его опытов страдает рядом недостатков, поэтому количественная интерпретация полученных результатов затруднена, но адсорбция Sr и Ва. Следует отметить, что авторы сами не придерживаются какой-либо определенной точки зрения на механизм изучаемых процессов и ограничиваются в отдельных работах полуэмпири-чегкими формулами, но качественно им удалось показать зависимость адсорбции от ряда факторов, в том числе рН раствора, концентрации радиоактивного изотопа, концентраций посторонних солей и др. Общий характер захвата радиоактивных изотопов гидратными осадками в зависимости от перечисленных факторов напоминает закономерности вторичной обменной адсорбции на полярных кристаллах. [41]
Рассмотрим вторичную обменную адсорбцию. Концентрирование следов элементов обычно производится в присутствии избытка осадителя, в результате чего частицы осадка имеют тот или иной заряд, обусловливающий соосаждение катионов или анионов. Однако нам хотелось бы отметить, что часто вторичная обменная адсорбция является первой стадией более глубоко идущего процесса. [42]
Переход макро - и микрокомпонентов из раствора в приповерх костный слой кристалла 5 называется потенциалобразующей ад сорбцией. Их переход в слой S или А путем замещения ионов на зывается обменной адсорбцией. Адсорбция во внутреннюю об кладку двойного слоя названа Ратнером первичной, а во внешнюк обкладку двойного слоя - вторичной адсорбцией. Таким образом различают первичную потенциалобразующую, первичную обмен ную и вторичную обменную адсорбцию на ионных кристаллах. [43]
Страницы: 1 2 3