Диспропор-ционирование
Cтраница 1
Окислительно-восстановительное диспропор-ционирование двух молекул альдегида здесь протекает в неводной среде под влиянием более слабого основания, чем в реакции Канниццаро - этилата алюминия. Механизм этой реакции выяснен. [1]
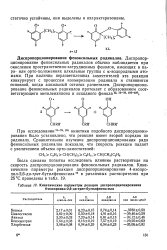 |
Кинетические параметры реакции диспропорционирования 4-изопропил - 2 6-ди-грег - бутилфеноксила. [2] |
Диспропор-ционирование феноксильных радикалов обычно наблюдается при окислении пространственно-затрудненных фенолов, имеющих в пара - или орто-положениях алкильные группы с - водородными атомами. При наличии неразветвленных заместителей эта реакция конкурирует с процессом изомеризации радикала и становится основной, когда алкильный остаток разветвлен. [3]
Диспропор-ционированию подвергается углеводород, а не сульфокислота, как это предполагали раньше. [4]
Реакция диспропор-ционирования этильных радикалов имеет стерический фактор на 10 - 4, что на порядок ниже его значения в предыдущей реакции. [5]
Поскольку вероятности для диспропор-ционирования и присоединения не сильно различаются для бутила и октила, это означает, что процесс присоединения тепловых атомов водорода к олефинам не важен при расходовании олефинов, за исключением этилена. [6]
При сложных радикалах возможны реакции диспропор-ционирования, которые идут с другими скоростями и дают свои продукты, что весьма осложнит применение способа определения относительных значений константы скорости и потребует отнесения скорости изучаемой реакции замещения: радикалов к суммарной скорости рекомбинации и диспро-порционирования их и знания скоростей этих реакций порознь. [7]
Химику часто приходится считаться с диспропор-ционированием ионов в растворе. Это явление часто приводит к тому, что некоторые степени окисления того или иного элемента в растворе оказываются неустойчивыми. В результате, например, марганец в водных растворах чаще всего бывает двух -, четырех - и семивалентным, остальные степени окисления обычно неустойчивы. [8]
Каталитические токи возникают также при диспропор-ционировании продукта электрохимической реакции R по следующей схеме. [9]
Хотя ускоряющее влияние кислотных агентов на диспропор-ционирование формальдегида известно довольно давно [1], подробные исследования этой модификации реакции были предприняты лишь в последние годы. В одной из первых работ [244] был найден дробный порядок по катализатору - серной кислоте. Подтверждением того, что кислотный катализ в данном случае действительно является специфическим, служит то, что эта корреляция не зависит от природы аниона кислоты. [10]
Подобно н-бутану роль ингибитора побочных реакций диспропор-ционирования играв - и н-пентан. Наиболее заметное влияние он оказывает при концентрации от 0 до 28 масс. % от н-гексана. При расчете состава полученных изоме-рияатов добавленный углваодород исключен. [11]
Между различными реакциями изомеризации и цепями диспропор-ционирования существует тонкое равновесие. Ингибиторы, подавляющие диспропорционирование пентана, нарушают это равновесие и сильно снижают реакцию диспропорционирования, не влияя в той же степени на реакцию изомеризации. Эти вещества вообще способны реагировать с карбоний ионом и ( или) с олефинами, регулируя их концентрацию. В этом отношении их функция сходна с действием буферов, применяемых для регулирования концентрации иона водорода в водных системах. [12]
Последний метод получения мономеров - реакцией диспропор-ционирования, основанный на перераспределении заместителей у атома кремния, ценен тем, что позволяет производить мономеры, которые другим путем получить либо невозможно, либо производство их связано с высокими энергетическими затратами. [13]
Несколько позже ( в главе Реакции диспропор-ционирования) мы рассмотрим вопрос о влиянии теплового эффекта реакции на ее направление более подробно. А пока, во-первых, посмотрим, откуда бе рется и куда девается та энергия, которая в виде теп - левого эффекта выделяется или поглощается химической системой. [14]
Данная реакция относится к типу реакций диспропор-ционирования. [15]
Страницы: 1 2 3 4