Равновесная адсорбция
Cтраница 2
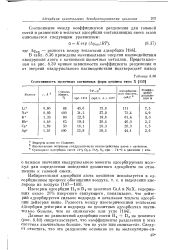 |
Селективность щелочных катионных форм цеолита типа X [ 1531. [16] |
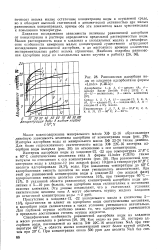
Данные по равновесной адсорбции смеси Н2 - ( - D2 на цеолитах ( рис. 8.40) свидетельствуют, что коэффициенты разделения в этих системах значительно больше, чем на угле или силикагеле. [17]
При определении равновесной адсорбции ПАВ на естественных образцах пород скорость фильтрации и длина модели существенного влияния не оказывают. Размеры модели выбирают таким образом, чтобы объем проб фильтрата раствора ПАВ, отбираемых гфиблизительно через 0 5 поровых объема прокачки, был достаточным для выполнения анализов проб. [18]
Меньшая величина равновесной адсорбции аммиака цеолитом I, содержащим практически одинаковое с цеолитом 2 количество кристаллической фазы в гранулах, обусловлена, по-видимому, меньшим количеством двухвалентных катионов в адсорбционных полостях цеолита I из-за меньшей степени ионного обмена ( ЗЗ масО у этого цеолита по сравнению с цеолитом 2 ( 67 % мае. [19]
Для описания равновесной адсорбции смесей н-парафинов с вытеснителями на цеолитах 5А можно применить уравнения Маркгема-Бентона [ I ], являющиеся результатом обобщения классической схемы Ленгмюра [1] в случае адсорбции смесей. [20]
Следовательно, уравнения равновесной адсорбции газов и паров в микропорах, широко применяемые в теории объемного заполнения микропор и являющиеся эмпирическими, могут быть теоретически обоснованы. [21]
Еще одна теория изотермической равновесной адсорбции основана на предположении об объемном характере заполнения микропористой структуры адсорбентов. [22]
Еще одна теория изотермической равновесной адсорбции основана на предположении об объемном характере заполнения микропористой структуры адсорбентов. Целевой компонент после его адсорбции считается подобным жидкой фазе, которая образуется при сжатии исходной паровой фазы адсорбтива под действием адсорбционных поверхностных сил. [23]
Важность развития термодинамики равновесной адсорбции газовых смесей очевидна. Действительно, огромное разнообразие свойств реальных твердых сорбентов и многокомпонентных адсорбтивов, наличие целой иерархии взаимосвязанных факторов, влияющих на процесс адсорбции, в значительной степени определяют преимущество термодинамического подхода, позволяющего получить важные сведения о поведении рассматриваемых систем без точного знания действующих в них сил. В то же время этому важному разделу термодинамики в литературе уделяется непропорционально меньшее внимание и многие вопросы термодинамики адсорбции смесей не нашли еще должного освещения. [24]
Значительные возможности для исследований равновесной адсорбции на поверхностях раздела фаз в методах Монте-Карло и молекулярной динамики предоставляет метод пробной частицы, используемый при расчетах химического потенциала компонентов системы. [25]
Имеющиеся экспериментальные данные по равновесной адсорбции и значениям Ds позволяют определить величину Ч в системах со слабой связью. При значениях Ds 10 - 4 - 10 - 6 см2 / с, характерных для систем со слабой связью ( см. разд. [27]
 |
Равновесная адсорбция воды из хладонов адсорбентами фирмы Linde ( США. [28] |
Диапазон исследования зависимости величины равновесной адсорбции от концентрации в растворе определяется предельной растворимостью воды Малая растворимость воды в хладонах и холодильных маслах и специфические особенности измерения малых концентраций существенно затрудняют исследования равновесной адсорбции, и до настоящего времени количество экспериментальных работ весьма ограничено. [29]
Рассмотрим выражение для величины равновесной адсорбции 6 для одного газа. А пропорционально его давлению в газовой фазе. [30]
Страницы: 1 2 3 4
