Обратимая волна
Cтраница 1
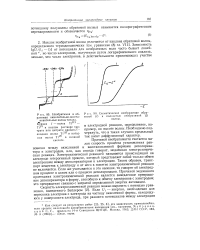
Отсюда обратимая волна симметрична относительно ее средней точки и характеризуется потенциалом Е / 2 полуволны. [1]
Обратимыми волнами называются волны, которые возникают при электродной реакции достаточно быстрой по сравнению с диффузией, так что на поверхности электрода всегда поддерживается равновесие. [2]
Потенциал полуволны обратимой волны является константой, характерной для каждого деполяризатора. Его величина не зависит ни от концентрации деполяризатора, ни от характеристик капилляра, ни от чувствительности гальванометра. Если же в результате электродного процесса образуется амальгама, то потенциал полуволны соответствует нормальному потенциалу амальгамного электрода ( см. разд. Если при постоянной чувствительности гальванометра изменять концентрацию одного и того же вещества, то при полярографировании получаются кривые, которые отличаются друг от друга высотой и потенциалом выделения ( см. гл. [3]
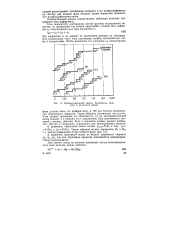 |
Полярографический спектр. Потенциалы полуволн в различных средах. [4] |
В уравнение обратимой волны не входят параметры скорости ( I D, & p, ос), так как обратимые процессы описываются закономерностями термодинамики. [5]
Другим случаем разделения обратимой волны является восстановление металлического иона из комплекса, когда в растворе нет избытка комплексо-образующего реагента ( см. гл. Как и раньше, рассмотрим конкретный пример. [6]
В отличие от обратимых волн потенциал полуволны необратимого процесса не является постоянной величиной. Как видно из формулы (51.16), неравновесный потенциал полуволны есть функция ipi - потенциала, а потому зависит от состава раствора. Кроме того, поскольку id зависит от параметров установки ( на вращающемся электроде - от скорости вращения, на капельном электроде - от скорости вытекания ртути и периода капанья), то соответственно от этих параметров будет зависеть и потенциал полуволны для необратимого процесса. [7]
В отличие от обратимых волн потенциал полуволны необратимого процесса не является постоянной величиной. Как видно из формулы (51.13), неравновесный потенциал полуволны является функцией - потенциала, а потому зависит от состава раствора. Соотношение CQ / ia, входящее в выражение для ф, не зависит от CQ. CQ - Кроме того, поскольку id зависит от параметров установки ( на вращающемся электроде - от скорости вращения, на капельном электроде - от скорости вытекания ртути и периода капанья), то соответственно от этих параметров будет зависеть и потенциал полуволны для необратимого процесса. [8]
В отличие от обратимых волн потенциал полуволны необратимого процесса не является постоянной величиной. Как видно из формулы (51.16), неравновесный потенциал полуволны есть функция ipi - потенциала, а потому зависит от состава раствора. Кроме того, поскольку id зависит от параметров установки ( на вращающемся электроде - от скорости вращения, на капельном электроде - от скорости вытекания ртути и периода капанья), то соответственно от этих параметров будет зависеть и потенциал полуволны для необратимого процесса. [9]
В отличие от обратимых волн потенциал полуволны необратимого процесса не является постоянной величиной. Как видно из формулы (51.16), неравновесный потенциал полуволны есть функция ipi - потенциала, а потому зависит от состава раствора. Кроме того, поскольку id зависит от параметров установки ( на вращающемся электроде - от скорости вращения, на капельном электроде - от скорости вытекания ртути и периода капанья), то соответственно от этих параметров будет зависеть и потенциал полуволны для необратимого процесса. [10]
Хлорофилл b дает одноэлектронную обратимую волну окисления, контролируемую диффузией. Вторая волна также обратима, но очень мала по высоте. Как считают, эта волна отвечает реакции катион-радикала хлорофилла Ь, состоящей в отщеплении магния с образованием нереакционноспособного продукта. [11]
Выше было рассмотрено применение обратимых волн ( простых ионов металла либо комплексов металла) для нахождения формальных и стандартных ОВ потенциалов. Реже с этой целью использовались квазиобратимые и необратимые полярографические волны, которые достаточно подробно проанализированы в работах [ 48; 53, с. [12]
Установлена корреляционная зависимость между потенциалами одноэлектронной обратимой волны восстановления нитрогруппы в вышеуказанных соединениях и 0 константами Джаффе по уравнению Е - Е п рла - Найдены значения трансмиссионные факторов ( я) для М но отношению к серии нитробензола. Для всех мостиков, кроме М - NH - , найденные значения я указывают на ослабление сопряжения заместителя с реакционным центром, которое зависит от природы мостика, характера сопряжения мостикового звена с бензольным ядром, содержащим реакционный центр и определяется строением изученных соединений. [13]
Кроме того, чтобы наблюдать обратимую волну, необходимо работать в хорошо забуферен-ном растворе. [14]
Страницы: 1 2 3 4