Форма - изотерма - адсорбция
Cтраница 3
Двумерная ассоциация адсорбированных ионов ПАВ не должна существенно отражаться на форме изотермы адсорбции и тем более на величине предельной удельной адсорбции, так как при этом не изменяется ориентация адсорбированных ионов. [31]
Статические ( вакуумные) и калориметрические методы измерения, позволяющие выявлять форму изотермы адсорбции и вид зависимости теплоты адсорбции от заполнения, также дают возможность судить об однородности поверхности. [32]
Особенности кинетики реакций на неоднородной поверхности не исчерпываются, однако, простым изменением формы изотермы адсорбции. Поверхность, неоднородная по теплоте адсорбции, должна быть неоднородна и кинетически. Будем считать, следуя Рогинскому [14], что в ходе процесса зависимость скорости реакции от концентраций реагентов остается неизменной на всех участках и температурная зависимость скорости реакции по-прежнему описывается уравнением Аррениуса. При этом величина предэкспонента постоянна на всех участках, а значение энергии активации распределено по некоторому закону. Все эти допущения являются дискуссионными, но в первом приближении они достаточны, так как главным эффектом действия катализатора обычно бывает именно изменение энергии активации реакции. [33]
Особенности кинетики реакций на неоднородной поверхности не исчерпываются, однако, простым изменением формы изотермы адсорбции. Поверхность, неоднородная по теплоте адсорбции, должна быть неоднородна и кинетически. [34]
Изотерма адсорбции является важной характеристикой системы адсорбент - адсорбат, так как знание формы изотермы адсорбции, а также взаимного расположения изотерм адсорбции различных веществ может помочь правильному выбору условий хроматографи-ческого разделения сложных смесей. [35]
Методами, которые служат для определения строения поверхности дисперсных веществ, являются: изучение формы изотермы адсорбции, определение дифференциальных теплот адсорбции и прогрессивное отравление катализаторов. В задачу настоящей статьи не входит детальный разбор всех результатов указанных исследований, и мы ограничимся только некоторыми примерами, чтобы продемонстрировать наличие значительных противоречий среди полученных экспериментальных данных. [36]
Как и следовало ожидать, при одинаковых адсорбционных параметрах влияние диффузного слоя гораздо сильнее сказывается на форме изотермы адсорбции заряженных частиц. [38]
При изучении адсорбционных явлений на границе раздела раст-зор ПАВ - твердое тело ярко проявляются особенности, связанные с формой изотерм адсорбции в области высоких концентраций ПАВ. [39]
 |
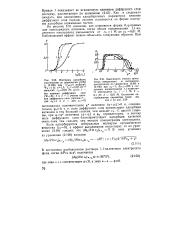
Ориентация молекул ПАВ на межфазной границе полярное твердое тело - водный раствор в условиях хемосорбции при малых ( а и больших ( 1 концентрациях. [40] |
При изучении адсорбционных явлений на границе раздела раствор ПАВ - твердое тело ярко проявляются особенности, связанные с формой изотерм адсорбции в области высоких концентраций ПАВ. [41]
Из уравнения ( 3) видно, что в первом приближении, когда выполняется соотношение ( 1), форма изотермы адсорбции при постоянном, потенциале не зависит от потенциала. [42]
Однако метод сравнения рассчитанных и экспериментальных кривых зависимости поверхностного давления от заряда электрода, как было впоследствии отмечено Парсонсом [28], является мало чувствительным к форме изотермы адсорбции. Значительно более чувствительной функцией является дифференциальная емкость электрода. АСд от Е при использовании изотерм адсорбции Генри, Фрейндлиха, Ленгмюра, Темкина и изотермы с вириаль-ными коэффициентами. Сопоставление полученных уравнений с экспериментальными данными по адсорбции на ртути молекул тиомочевины [127] и н - С5НиОН [177] показало, однако, что исследованные изотермы адсорбции лишь в первом приближении могут быть использованы для описания опытных С, Е - кривых. [43]
Об этом свидетельствовали не только экспериментальные данные по кинетике контактных реакций, но и наблюдения по отравлению катализаторов, данные о скорости адсорбционных процессов и даже форма изотерм адсорбции в широком интервале изменения концентраций. [44]
Таким образом, уменьшение содержания катионов Li при переходе от цеолита LiNaX к цеолиту LiNaY приводит не только к снижению адсорбции, но и к изменению формы изотермы адсорбции. Форма зависимости д от ns в случае цеолита LiNaX также иная: q в начальной области уменьшается с ростом ns, так как неравноценность адсорбционных центров в этом случае оказывает большее влияние на теплоту адсорбции, чем взаимодействие адсорбат - адсорбат. [45]
Страницы: 1 2 3 4