Форма - кривая - титрование
Cтраница 1
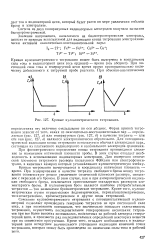 |
Кривые кулонометрического титрования. [1] |
Форма кривой титрования зависит от того, какая из окислительно-восстановительных пар - определяемая ( рис. 127, а) или генерируемая ( рис. 127, б) в качестве титранта - или обе они ( рис. 127, в) являются электрохимически обратимыми. Для потенциоке-трической индикации конца титрования используется обычная электродная пара, состоящая из платинового индикаторного и каломельного электродов сравнения. [2]
Форма кривой титрования определяется характером конфор-мационного перехода. Если конформационный переход некоопе-ративен и описывается уравнением мономолекулярной реакции ( 25), то кривые титрования макромолекулы в области перехода имеют такую же форму, как и кривые титрования чисто спиральной и чисто клубкообразной молекул ( если форма этих кривых одинакова), но лежат между ними. [3]
Форма кривой титрования одинакова для различных концентраций n - уразина. Установлено, что черный осадок содержит 97 % металлического серебра. Это показывает, что при титровании имеет место окислительно-восстановительная реакция, в результате которой ионы серебра восстанавливаются до металла. [4]
Форма кривой титрования определяется характером конфор-мацио иного перехода. Если конформационный переход некоопе-ративен и описывается уравнением мономолекулярной реакции ( 25), то кривые титрования макромолекулы в области перехода имеют такую же форму, как и кривые титрования чисто спиральной и чисто клубкообразной молекул ( если форма этих кривых одинакова), но лежат между ними. [5]
Форма кривой титрования зависит от того, какое вещество электроактивно до и после к. Обычно кривая состоит из двух линейных участков, пересечение которых соответствует к. [6]
Форма кривой титрования зависит также от прочности связи X и R в продукте реакции XR. Скачкообразное изменение концентрации определяемого вещества вблизи точки эквивалентности значительно больше, если диссоциация продукта реакции очень мала или практически отсутствует. На рис. 7.2 сопоставлены две кривые титрования 0 1 М растворов X 0 1 М растворами реагентов R и С. Из сравнения кривых видно, что скачок концентрации вблизи точки эквивалентности зависит от константы, характеризующей продукт реакции: он тем больше, чем больше константа устойчивости, или, что то же самое, чем больше прочность соединения, образующегося в результате взаимодействия. Большой скачок благоприятно сказывается на точности титрования. [7]
Форму кривой титрования легко предсказать. Концентрацию каждого иона в последовательных точках при титровании вычисляют известными методами, основанными на законах стехиометрии, равновесия и разбавления. Для примера на рис. 18 - 5 показано титрование НС1 раствором NaOH. [9]
Изучение формы кривой титрования вообще может дать представление только о существовании определенных термодинамических равновесных состояний, но не о фактическом пути реакции. [10]
Иногда форму кривой титрования и тем самым протекание процесса титрования можно заметно улучшить, изменяя соответствующим образом состав раствора и условия эксперимента. Например, реальные потенциалы многих полуреакций изменяются при изменении концентрации кислоты или некоторого комплексующего агента. [11]
Если известны форма кривой титрования и строение растворенного вещества, на основе значений рКа можно предсказать возможность раздельного определения соединений в смесях. Смеси аминов легче поддаются дифференциальному определению, чем смеси амидов или замещенных мочевин. [12]
Если известны форма кривой титрования и строение растворенного вещества, на основе значений рКа можно предсказать возможность раздельного определения соединений в смесях. Смеси аминов легче поддаются дифференциальному определению, чем смеси амидов или замещенных мочевин. [13]
Внимательно рассмотрите форму кривой титрования и положение точки эквивалентности. Для расчета объема титранта, соответствующего точке эквивалентности, следует ввести по команде значения концентраций обоих растворов и объем титруемого раствора. [14]
Очевидно, что форма кривой титрования будет определяться характером взаимодействия титруемого и рабочего растворов. Рассмотрим основные типы кривых титрования. [15]
Страницы: 1 2 3 4
