Форма - кривая - титрование
Cтраница 2
Факторы, влияющие на форму кривой титрования. Величина скачка титрования определяет правильность обнаружения точки эквивалентности. Что касается кривой титрования, изображенной яа рис. 8 - 1, то существуют два фактора, которые влияют яа скачок этой кривой титрования в области точки эквивалентности: во-первых, исходная концентрация ( раствора хлорида, во-вторых, константа равновесия ( соответствующая произведению растворимости) реакции титрования. [16]
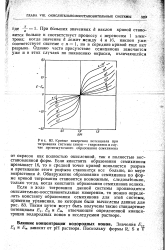 |
Кривые измерения потенциала при титровании системы хинон - гидрохинон в случае промежуточного образования семихинона. [17] |
Обнаружение образования семихинона по форме кривой титрования становится возможным, следовательно, только тогда, когда константа образования семихинона велика. Таким путем могут быть получены также стандартные потенциалы Elt Ег и Ет отвечающие определенной концентрации водородных ионов в исследуемом растворе. [18]
При титровании более разбавленных растворов форма кривой титрования одной и той же кислоты изменяется, так как увеличивается степень ее диссоциации. [19]
 |
Кривые хронокондуктометрического титрования раствором NaOH 0 075 н. растворов. [20] |
Поэтому значение этой суммы обусловливает форму кривой титрования соли. [21]
Потенциометрический метод индикации хелонометрического титрования прямо дает форму кривой титрования рМ / ( а), так как потенциал индикаторного электрода представляет собой меру активности иона металла, не вступившего в реакцию комплексооб-разования. [22]
Влияние различных видов катионов на положение и форму кривой титрования обусловлено лишь изменениями константы равновесия реакции замещения иона водорода в обменном комплексе. [23]
X и концентрации реагента R влияет на форму кривой титрования. Видно, что высота скачка вблизи точки эквивалентности меньше, чем для более концентрированных растворов, и кривая идет уже не вертикально, а становится более пологой. Далее будет показано, что это отрицательно сказывается на правильном установлении точки эквивалентности и на точности определения. [24]
Изменение плотности тока на электродах сказывается на форме кривой титрования, а при более высоких плотностях максимум, кроме того, смещается. Так как пары электродов, приготовленные в одинаковых условиях, могут иметь различную активную поверхность, нужно определять оптимальный потенциал для данного высоко-омного сопротивления; для электродов из платиновой проволоки площадью 5 мм2 ( диаметр 0 5 мм, длина 3 Л1Л1), посеребренных и бромированных по методике, описанной в разд. [25]
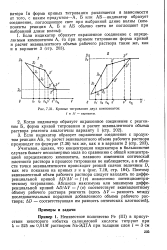 |
Кривые титрования двух компонентов. / и / / - варианты. [26] |
Когда индикатор образует окрашенное соединение с реагентом Б, форма кривой титрования и расчет эквивалентного объема раствора реагента аналогичны варианту 1 ( стр. [27]
По мере уменьшения силы титруемой кислоты наблюдается заметное изменение формы кривой титрования до точки эквивалентности. Это обусловлено, как и можно было предположить, различиями в степени диссоциации кислот. В случае борной кислоты, константа диссоциации которой настолько мала, что кислота в исходном растворе практически не диссоциирована, наблюдается линейное увеличение электропроводности от нуля до конечной точки, по мере того как в результате реакции нейтрализации образуется ионизованная соль, борат натрия. В случае хлоруксусной и уксусной кислот играют роль два конкурирующих процесса, которые приводят к появлению минимума на кривой электропроводности. В исходном растворе вследствие некоторой диссоциации этих кислот присутствуют ионы Н, обладающие высокой эквивалентной электропроводностью. [28]
Константа диссоциации меняется с температурой, что влияет на форму кривой титрования. Изменение температуры влияет также на окраску индикатора. Поэтому необходимо титровать всегда при одной температуре и при этой же температуре устанавливать концентрацию стандартного рабочего раствора. Чаще всего титруют при комнатной температуре. [29]
Задача химика-аналитика состоит главным образом в том, чтобы найти форму кривой титрования. [30]
Страницы: 1 2 3 4