Форма - потенциальная кривая
Cтраница 2
На рис. 18 приведена схема каталитического процесса в форме соответствующих потенциальных кривых. [17]
Как показывает анализ этого вопроса, существенное значение имеет форма потенциальной кривой вандерваальсовского взаимодействия молекул данного вещества. [18]
Центральным моментом обзора является обсуждение двух-центрового приближения для расчета формы потенциальных кривых в промежуточных комплексах каталитических реакций. Оно проделано на примере элементарной стадии переноса протона в гетерогенном кислотном катализе, где активными центрами служат поверхностные гидроксильные группы, обладающие высокохарактеристическими валентными колебаниями. Вследствие малой массы протона и угловой структуры группировок М - О - Н их потенциальные кривые хорошо описываются простейшей моделью ангармонического осциллятора. [19]
Введение изотопа ( например, в углеводороды) не меняет форму потенциальной кривой, но смещает уровень нулевой энергии. [20]
 |
Потенциальные кривые для ДВУХ однотипных реакций. [21] |
Если реакции однотипны, то на диаграммах условный путь реакции и форма потенциальных кривых примерно одинаковы. Как видно, при этом высота энергетического барьера прямой реакции действительно уменьшается на определенную долю си от значения общего смещения кривой. [22]
При взаимодействии адсорбированных молекул с более кислыми, чем на поверхности силикагеля, ОН-группами форма потенциальных кривых искажается сильнее. [23]
Для двухъядерной системы может осуществляться, вообще говоря, три рода электронных состояний, отличных по форме потенциальных кривых. [24]
Анализ кривых межмолекулярного взаимодействия для молекулярных пар показывает, что электростатическая часть здесь играет значительное меньшую роль, и характер связи и форм потенциальных кривых определяются в основном эффектами, связанными с перераспределением электронной плотности. [25]
Является ли причиной уширения большая поляризуемость и какие взаимодействия осуществляются при этом, неясно, поскольку экспериментальные результаты находятся в противоречии с формой потенциальной кривой в этих водородных связях. Шульман [238] постулировал потенциальную функцию с двумя минимумами, при этом протон, находящийся в первом возбужденном состоянии, может переходить от тимина к аденину. Квантовомеханические расчеты [268 - 271] приводят к противоположным выводам о форме потенциальной ямы. Следует, однако, учесть, что пары оснований при этих расчетах рассматривались изолированно от окружающей среды. Гидратация ДНК и стопкообразная упаковка пар оснований оказывают определяющее влияние на форму потенциала водородных связей. [26]
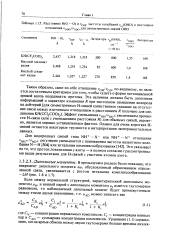 |
Расстояние R ( O - - - О и гон, частоты колебаний cas ( OHO и изотопные отношения пно ою аля симметРичных связей ОНО. [27] |
Таким образом, само по себе отношение OH / VOD, по-видимому, не является достаточным критерием для того, чтобы судить о форме потенциальной кривой вдоль координаты протона. Эффект уменьшения / OH / / OD c увеличением прочности Н - связи ( или с уменьшением расстояния R) для обычных связей, вероятно, является хорошо установленным фактом. Однако для очень коротких Н - связей остаются некоторые трудности в интерпретации экспериментальных данных. [28]
Однако при возбуждении пары оснований электрон переходит от уровня гуанина на уровень цитозина ( 0 99 ег) и возникает заметная поляризация, отражающаяся на форме потенциальной кривой протона в водородной связи. Первый уровень возбужденной кривой является уже туннельным для протона. Это значит, что возбуждение ( например, действием УФ-излучения) создает условия, в которых вероятности образования нормальных и таутомерных форм оснований одинаковы. Таутомерные формы в цепи ДНК могут дать начало образованию различных мутаций. [29]
На рис. 33 изображена, конечно, только схема, не позволяющая предсказать величину активационного барьера, так как неизвестно, при какой степени сближения частиц происходит переход, поскольку сама форма потенциальных кривых изменяется в системе, состоящей из трех атомов. [30]
Страницы: 1 2 3 4
