Форма - потенциальная кривая
Cтраница 3
Рн - энергия связи атома водорода с металлом электрода ( адсорбционный потенциал); R - газовая постоянная; Т - абсолютная температура; р - коэффициент ( меньше единицы), характеризующий форму потенциальной кривой для связи Me - Н; va - константа, зависящая от природы восстанавливающегося вещества. [31]
Наиболее вероятные электронные переходы этих молекул характеризуются полным отсутствием или очень малым тепловым рассеянием энергии, что определяется постоянством или незначительным изменением квантового колебательного числа при электронном возбуждении молекулы. Такая форма потенциальных кривых обычно не приводит к диссоциации молекулы в результате поглощения фотона, так как согласно принципу Франка - Кондона ( см. § 3 - 2) невозможен электронный переход в зону диссоциации с низкого уровня колебательной энергии молекулы в невозбужденном состоянии. [32]
Находясь в возбужденном электронном состоянии, молекула имеет иные свойства, чем тогда, когда она находится на нулевом электронном уровне. Меняется и форма потенциальной кривой, а вместе с ней и равновесные расстояния между атомами. [33]
Для тяжелых ядер форма потенциальной кривой близка к прямоугольной потенциальной яме. [34]
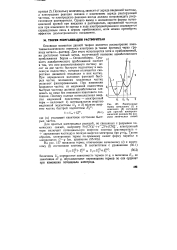 |
Электронные термы начального ( / и конечного ( 2 состояний для простой электрохимической реакции без раз-где ( а указывает квантовое состояние быст - рыва химических связей рых частиц. [35] |
Поскольку величина qa зависит от заряда введенной частицы, а электродная реакция связана с изменением заряда реагирующей частицы, то электродную реакцию всегда должна сопровождать реорганизация растворителя. Однако вывод о неизменности формы потенциальной кривой при введении в растворитель заряженной частицы или при изменении ее заряда в ходе электродной реакции оказывается справедливым лишь в первом приближении, если можно пренебречь эффектом диэлектрического насыщения. [36]
 |
Кривые потенциальной энергии для реакции свободнорадикаль-ного замещения Н - Н2 - - Н2 Н -. [37] |
Для радикального замещения этот эффект не очень важен, так как точка пересечения потенциальных кривых расположена низко, а энергии активации обычно не превышают 20 - 30 кДж / / моль. Для молекулярных же реакций изменение формы потенциальных кривых может быть гораздо существеннее, в результате чего расчет энергии активации с помощью модели невозмущенных кривых может стать просто неверным. Особенно существенно это обстоятельство в катализе, поскольку форма кривых изменяется уже на стадии адсорбции или образования промежуточных комплексов. [38]
Такое изменение скорости является результатом иного энергетического состояния участников реакции разряда. Это отражается на положении и форме соответствующих потенциальных кривых. Возникший скачок потенциала может влиять на обе потенциальные кривые. [39]
Приведенные формулы, как уже отмечалось, справедливы только для малых амплитуд колебаний, или, что то же самое, для малых квантовых чисел. Для более высоких возбужденных состояний отклонение формы потенциальной кривой от параболы приводит к тому, что колебания уже нельзя более считать гармоническими. В формулы, - выведенные выше, необходимо внести поправки, которые меняют величины термов. При увеличении квантового номера s уровни все более и более сгущаются, пока ие будет достигнута так называемая граница вхождения ( фиг. Эта граница соответствует диссоциации молекулы, прячем необходимая для нее энергия равна глубине потенциальной ямы, отсчитываемой от асимптотического предельного значения потенциала. Эта энергия равна V ( oo) - К ( г0), и если сообщить молекуле такую, или ббльшую энергию, то она распадается на атомы, или иоиы, причем они разлетятся с определенными скоростями, определяемыми избытком сообщенной энергии по сравнению с энергией диссоциации. [40]
В случае фазовых переходов второго рода между различными кристаллическими модификациями происходит или смещение подрешеток кристалла в направлении одного из нормальных колебаний, или упорядочение положения подрешеток вдоль некоторых колебаний. При этом оказывается, что существенное значение имеет форма потенциальной кривой нормального колебания. В случае потенциала с одним минимумом фазовый переход является переходом типа смещения, в случае двух минимумов - типа порядок - беспорядок. [41]
Так же, как и выше, следует иметь в виду, что координата реакции перехода протона зависит от других межъядерных расстояний в комплексе. Было показано, что в обоих случаях параметры и форма потенциальной кривой V ( г) очень чувствительны к изменению величины R - расстояния между тяжелыми ядрами. Изменение R на величину менее 0 1 А приводит к появлению двух симметричных ям, разделенных барьером. Яношек f71 ] предполагает, что именно такая ситуация может иметь место при переходе от изолированного иона Н5С2 к его водному раствору. [42]
Так же, как и выше, следует иметь в виду, что координата реакции перехода протона зависит от других межъядерных расстояний в комплексе. Было показано, что в обоих случаях параметры и форма потенциальной кривой V ( г) очень чувствительны к изменению величины R - расстояния между тяжелыми ядрами. При значениях R, соответствующих наиболее устойчивой конфигурации, кривые симметричны и имеют один минимум, соответствующий центральному положению протона. Изменение R на величину менее 0 1 А приводит к появлению двух симметричных ям, разделенных барьером. Яношек [71] предполагает, что именно такая ситуация может иметь место при переходе от изолированного иона H50jf к его водному раствору. [43]
Как известно из накопленного огромного материала по ИК-спектрам и точным расчетам колебаний в сложных молекулах [25], к таким характеристическим группировкам относятся двойные связи С С, группировки C N, карбонильные группы и, в первую очередь, гидроксильные группы, играющие роль активных центров в реакциях кислотного катализа. Именно для них и имеются наиболее детальные сведения о форме потенциальных кривых и характере ее изменения в ходе каталитических реакций. Рассмотрим эти данные более подробно. [44]
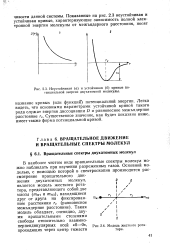 |
Неустойчивая ( а и устойчивая ( б кривые потенциальной энергии двухатомной молекулы.| Модель жесткого ротатора. [45] |
Страницы: 1 2 3 4