Форма - кинетическая кривая
Cтраница 1
Форма кинетических кривых зависит от точности измерений, в особенности на ранних стадиях реакции, тогда как время достижения образцом температуры реакции ( или других параметров реакции) обычно плохо определено. [1]
Изменения формы кинетических кривых под влиянием различных факторов или различных способов обработки могут служить указанием на изменения кинетического режима протекания реакции. Специально подобранные воздействия насто позволяют получить ценные сведения о механизме реакции. [2]
Известно, что форма кинетических кривых необязательно соответствует определенному механизму, хотя и позволяет сузить число возможных вариантов. [3]
Чтобы объяснить такую форму кинетических кривых, необходимо принять, что ядра образуются в результате бимолекулярной реакции активных частиц, концентрация которых увеличивается с постоянной скоростью, причем этот процесс происходит на потенциальных центрах, число которых вначале постоянно. [4]
С значительно меняет форму кинетической кривой ( см. рис. 210, кривая 3): в начале реакции наблюдается падение давления. В продуктах обнаружен ацетон. Более подробных данных не приводится. [5]
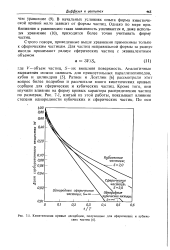 |
Кинетические кривые десорбции, полученные для сферических и кубических частиц. [6] |
В начальных условиях опыта форма кинетической кривой мало зависит от формы частиц. Однако по мере приближения к равновесию такая зависимость усиливается и, даже используя уравнение ( 10), приходится более точно учитывать форму частиц. [7]
Согласно ( 20), форма кинетических кривых Q ( t) определяется отношением W2 / Ws. При W2 / Ws l отношение Q ( t) / Qe возрастает от начального значения, равного 1 при Ws Cl, когда в раствор эмиттированы электроны, но восстановление Н - атомов не успело произойти, до Q ( t) / Qe2 при Wst, когда в раствор дополнительно переходит заряд Qe в результате электрохимической десорбции. Когда W2 / Wsh Q ( t) / Qe при tt0, поскольку из-за равенства скоростей ионизации и электрохимической десорбции эти процессы не изменяют эмиттированный заряд. При W2 / Ws l отношение Q ( t) / Qe уменьшается ( от 1 при W2 ( t) до 2WS / W2 при W2 ( t) -) вследствие возвращения электронов в электрод при ионизации Надс. [8]
Как и в случае вулканизации НК, форма кинетических кривых резко изменяется в зависимости от температуры. При 143 С в области 40 - 60 мин имеется максимум. При 160 и 180 С наблюдается только спад Е со временем вулканизации. [9]
Полученные зависимости W ( t) однотипны по форме кинетических кривых. Время установления сорбционного равновесия тем больше, чем больше ф: для нитроаммофоски оно равно 4 - 5 ч при ффкр и 10 - 25 ч при ффкр. При больших значениях Ф гигроскопичные образцы водорастворимых солей и удобрений после достижения определенной влажности образца расплываются и постепенно переходят в жидкое состояние еще до достижения сорбционного равновесия. [10]
На рис. 7 показано, каким образом на форме кинетических кривых отражается варьирование значений констант скоростей различных стадий. Изменение / с ф в основном сказывается на начальном участке кривой, Ам - на участке максимальной скорости, a kr - па конечной стадии процесса. Это обстоятельство существенно упростило подбор констант и позволило однозначно установить такую их комбинацию, при которой расчетные кинетические кривые наилучшим образом соответствовали экспериментальным. [11]
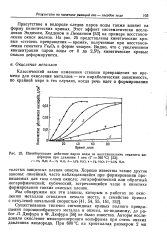 |
Ингибирующее действие паров воды на восстановление гематита водородом при давлении 1 атм ( Г395 С. [12] |
Присутствие в водороде следов паров воды также влияет на форму кинетических кривых. Этот эффект систематически исследован Эндомом, Хедденом и Леманном [53] на примере восстановления окиси железа. На рис. 25 представлены кинетические кривые степень превращения - время, полученные при восстановлении гематита РеуОз в форме чешуек. Видно, что с увеличением концентрации паров воды от 0 до 2 5 % кинетические кривые сильно деформируются. [13]
Кроме того, в табл. 3.1 подчеркивается очень важная проблема формы кинетических кривых при низких степенях превращения. Эта форма зависит от закона зародышеобразования ( степенного, экспоненциального или мгновенного) и закона роста зародышей. Эти закономерности и их различные сочетания детально изложены в гл. [14]
При разложении в атмосфере водорода или гелия при низком давлении ни форма кинетической кривой, ни энергия активации не изменяются, при этом, однако, константа скорости больше, чем при разложении в вакууме. Фланаган исследовал также влияние паров воды на скорость дегидратации и на природу дегидратированного продукта и нашел, что зависимость скорости дегидратации от давления паров воды при 120 описывается кривой с максимумом. Кривые такой общей формы, на которых скорость проходит через один или несколько максимумов, обсуждаются ниже в настоящей главе. [15]
Страницы: 1 2 3 4