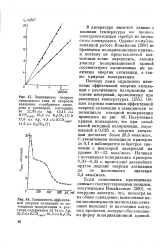
Форма - поляризационная кривая
Cтраница 3
Тедорадзе и Асатиани [240, 241] нашли, что природа аниона фона оказывает влияние на положение и форму поляризационных кривых, снятых на ртутном электроде в кислых растворах и-толуи-дина и трибензиламина. Указанные авторы объяснили это явление совместным действием анионов и адсорбирующихся на электроде названных выше ароматических аминов на строение двойного электрического слоя, что в зависимости от условий вызывает облегчение или затруднение разряда ионов водорода. Однако, по нашему мнению [104. 242], Тедорадзе и Асатиани наблюдали проявление специфического анионного эффекта при каталитическом выделении водорода. В отличие от уже цитированных работ Гирста, а также работы [239], где в качестве адсорбирующихся катионов брались тетразамещенные производные аммония, Тедорадзе и Асатиани использовали амины, имеющие свободный водород и, следовательно [12], могущие вызывать каталитическое выделение водорода. [31]
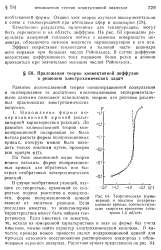 |
Теоретическая ( пунктирная и опытная поляризационные - кривые, соответствующие скорости вращения электрода 1 5 обIсек. [32] |
В случае необратимых реакций, идущих со скоростью, сравнимой со скоростью подачи реагентов к поверхности, форма поляризационной кривой зависит от кинетики реакции. Если последняя известна, то вольтамперная Уарактеристика может быть найдена теоретически. [33]
По-видимому, есть возможность оценки склонности к структурной коррозии, связанной с образованием а-фазы, по изменению формы поляризационной кривой при переходе из пассивной области в транспассивную и в область вторичной пассивности. Это позволяет заключить, что указанные фазы оказывают решающее влияние при структурных типах коррозии нержавеющих сталей в азотной кислоте высоких концентраций в условиях высоких температур или давлений. Присутствие в структуре хромоникелевых сталей феррита, эвтектических карбидов или других фаз усиливает коррозию в азотной кислоте. [34]
Если в фосфатном электролите хлористый аммоний заменить бензойной кислотой, то, как видно из рис. 101, форма поляризационной кривой несколько изменяется. В данном случае границы между отдельными ветвями становятся менее четкими и на кривых проявляется меньше участков. Этим, очевидно, следует объяснить сделанный некоторыми исследователями вывод [311], что кривая катодной поляризации палладия в фосфатном электролите состоит только из трех отдельных ветвей. [35]
 |
Отношение функция параметра А / г. [36] |
Если необратимая химическая реакция ( первого порядка) протекает с небольшой скоростью, то она практически не влияет на форму поляризационной кривой. [37]
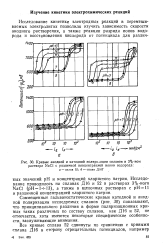 |
Кривые анодной и катодной поляризации сплавов в 3 % - ном растворе NaCl с различной концентрацией ионов водорода. [38] |
Совмещенные гальваностатические кривые катодной и анодной поляризации исследуемых сплавов ( рис. 30) показывают, что принципиального различия в форме поляризационных кривых таких различных по составу сплавов, как Д16 и 52, не отмечается, хотя имеются некоторые специфические особенности, заслуживающие внимания. [39]
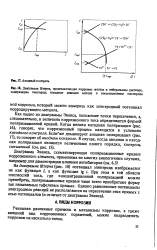 |
Анодный контроль.| Диаграмма Штерна, представляющая коррозию железа в нейтральном растворе, содержащем кислород. катодная реакция состоит в восстановлении кислорода. [40] |
Как видно из диаграммы Эванса, положение точки пересечения, а, следовательно, и величина коррозионного тока определяются формой поляризационной кривой. Когда велика катодная поляризация ( рис. 16), говорят, что коррозионный процесс находится в условиях катодного контроля. Если же доминирует анодная поляризация ( рис. 17), то говорят об анодном контроле. [41]
Такие уравнения находят достаточно широкое применение; действительно, чем бы ни была обусловлена необратимость процесса, стадии, следующие за выражением ( 1), уже не оказывают влияния на форму поляризационной кривой. [42]
Добавление сероводорода до 0 935 об. % в производственный газ, пропускаемый во время опыта через оборотную воду со значением рН 7 6, практически не сказывается на токе саморастворения и форме поляризационных кривых. [43]
Если сопоставить приведенные данные с соответствующими данными, полученными Измайловым [260], то нетрудно заметить, что, несмотря на их общее совпадение, выявленные нами закономерности значительно отчетливее передают те изменения катодных процессов, которые обусловливают форму поляризационной кривой. [45]
Страницы: 1 2 3 4