Форма - поляризационная кривая
Cтраница 4
Электрохимические способы зашиты основаны на разных принципах: а) нанесение на поверхность корродирующего металла защитного гальванопокрытия - тонкого слоя коррозионно более стойкого металла; б) электрохимическое оксидирование поверхности или нанесение других видов поверхностных слоев; в) воздействие на поляризационные свойства корродирующего металла ( положение и форму поляризационных кривых); г) воздействие на потенциал корродирующего металла. [46]
Поляризацию рабочего электрода осуществляют линейно изменяющимся напряжением с малой ( 0 1 - 5 мВ / с) или большой ( 0 01 - 100 В / с) амплитудой. Форма поляризационной кривой зависит от поляризующего напряжения. [47]
Равенство ( 2) означает, что поляризационная кривая не одинакова на всей поверхности образца, а меняется при переходе от одной точки микрорельефа к другой. Причиной изменения формы поляризационной кривой в точках, расположенных во впадинах и на выступах, служит различие в концентрации разряжающихся ионов, ионов комплексообразователя или поверхностно-активной добавки, диффундирующей к электроду и расходующейся при электролизе, разная толщина образовавшихся окисных пленок или пленок, составленных из продуктов электролиза и др. В зависимости от причин, вызвавших местные отличия в форме поляризационных кривых, поляризация может в одних случаях расти, а в других уменьшаться в направлении от впадины к выступу. Направление изменения поляризации определяет и характер самого явления. Например, для случая выравнивания поляризация IB направлении выступов растет, а для случая отрицательного выравнивания наоборот - падает. [48]
Кривую, выражающую графическую зависимость поляризации от плотности тока, называют поляризационной кривой. Вопрос о форме поляризационной кривой для того или иного конкретного случая не является простым. Этот вопрос усложняется явлениями одновременного действия ряда замедленных процессов, переменной и по-разному зависящей от плотности тока долей их участия в общей поляризации. Следует иметь в виду также то, что известные типы поляризации пока не до конца изучены и что, по-видимому, существуют виды поляри-ризации, еще не известные нам. [49]
Для этого снимаются анодные и катодные поляризационные кривые. В общем случае анализ формы поляризационных кривых и изучение характера их зависимости от состава раствора, температуры, ингибирующих добавок позволяют получить довольно полные сведения о природе изучаемого электрохимического процесса. В зависимости от того, как влияют на кинетику электрохимической реакции конкретные ингибиторы и в какой степени замедляют ее, их делят на анодные, катодные или смешанные. [50]
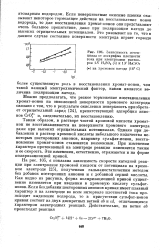 |
Зависимость потенциала от логарифма плотности тока при электролизе растворов IN H2SO4 ( о и IN HaCrO. [51] |
На рис. 105, а показана зависимость скорости катодной реакции при электролизе хромовой кислоты от потенциала на хромовом электроде [25], полученная гальваностатическим методом без добавок посторонних анионов и с добавкой серной кислоты. Как видно из рисунка, форма поляризационной кривой существенно изменяется при введении в хромовую кислоту сульфат-ионов. Если без добавки посторонних анионов кривая имеет плавный характер и на электроде во всем интервале плотностей тока происходит выделение водорода, то в присутствии сульфат-ионов кривая состоит из двух дискретных ветвей ab и cd, отличающихся характером электродных реакций. [52]
В этой главе неоднократно упоминалась поляризация. Многие факторы оказывают влияние на форму поляризационной кривой. Непосредственные электрохимические особенности описаны в разд. Было также рассмотрено устройство электродов, в частности датчика. В этом же разделе было кратко описано влияние загряз-няющих примесей на возникновение значительных токов локального действия. [53]
Данные о поляризации катода при восстановлении хромовой кислоты разнообразны и противоречивы, что можно объяснить, с одной стороны, нестабильностью поляризации во времени, а с другой стороны, недостаточно строгим поддержанием постоянства силы тока или напряжения в цепи. Как видно из этих рисунков, форма поляризационных кривых имеет весьма разнообразный вид. [54]
Когда приступают к анализу исходных данных с точки зрения выявления возможности моделирования, то имеют дело с поляризационными кривыми, выраженными в размерных единицах поляризации и плотности тока. В общем случае от величины масштабов зависит форма безразмерных поляризационных кривых. Выбор масштабов должен быть, очевидно, осуществлен в процессе анализа исходных данных. Рассмотрим с точки зрения подхода к моделированию наиболее часто встречающиеся на практике случаи, когда граничными условиями противоположного электрода можно пренебречь. [55]
Необходимость включения Дк Ср иДа срв условия однозначности связана с изменением формы безразмерной поляризационной кривой, а следовательно, и граничных условий при перемене средней плотности тока. [56]
Электрохимическая реакция протекает обычно через различные стадии, которыми могут быть, например, подвод реагирующего компонента в зону реакции за счет диффузии из объема раствора или за счет образования его по какой-то химической реакции в объеме, собственно электрохимическая стадия, связанная с получением или отдачей электронов металлической фазе, отвод образующихся продуктов из зоны реакции как за счет простой диффузии, так и за счет последующей химической реакции в объеме. Естественно, что характер зависимости скорости реакции от потенциала ( то есть форма поляризационной кривой) будет определяться тем, какая из перечисленных стадий лимитирует ее скорость. [57]
Но во всех случаях эти реакции и скорость их протекания должны определяться положением и формой поляризационных кривых. Поэтому для рассмотрения электролиза нужно разобрать некоторые типичные случаи, пользуясь поляризационными кривыми. [58]
Поверхность графита покрыта окислами, количество и состав которых существенно зависят от предыстории образца. Это ведет к плохой воспроизводимости результатов как по величине перенапряжения, так и в отношении формы поляризационной кривой. При этом исходные поверхностные окислы постепенно удаляются и образуется новая поверхность в некотором стационарном состоянии окисления, которое при дальнейшем электролизе уже практически не меняется. Обработанные таким образом электроды и использовались в наших экспериментах. Опыты проводились в сильнокислых растворах, в которых выделение кислорода сведено на нет, так что анодный ток соответствовал только одному процессу - выделению хлора [ 295, ср. [59]
Страницы: 1 2 3 4