Форма - электрокапиллярная кривая
Cтраница 2
Теория Штерна позволяет правильно истолковать зависимость формы электрокапиллярной кривой от концентрации и природы присутствующих электролитов, хотя, как это было показано О. А. Есиным и Б. Ф. Марковым ( эффект Есина - Маркова), она и не обеспечивает количественной сходимости с опытом. [16]
Добавление неорганических электролитов приводит к изменению формы электрокапиллярной кривой. Максимум электрокапиллярной кривой смещается при этом в катодную область. Особенно велика адсорбционная способность крупных органических анионов анионных ПАВ. [17]
Определяют влияние поверхностно активных веществ на форму электрокапиллярной кривой. Снимают электрокапиллярную кривую для ртути в 0 5 М растворе Na2SC4, в 0 5 М растворе Na2SO4 1 М пропионовой кислоты, а затем в 0 5 М растворе Na2SO4, насыщенном масляной кислотой. [18]
Неионогенные ПАВ также могут сильно влиять на форму электрокапиллярной кривой: они способны к адсорбции при умеренных потенциалах как на анодной, так и на катодной ветвях электрокапиллярной кривой. При больших ( как положительных, так и отрицательных) потенциалах ди-польные молекулы воды настолько сильно притягиваются к поверхности, что вытесняют молекулы неионогенных ПАВ. Поэтому неионогенные ПАВ понижают поверхностное натяжение только в средней части электрокапиллярной кривой. [19]
Определяют влияние концентрации поверхностно активных веществ на форму электрокапиллярной кривой. [20]
 |
Строение двойного слоя ( а и распределение потенциала в двойном слое ( б по теории Гельмгольца.| Строение двойного слоя ( а и распределение потенциала в двойном слое ( б по теории Гун - Чапмена. [21] |
Таким образом, теория Гельмгольца позволяет качественно объяснить форму электрокапиллярной кривой, а в отдельных случаях, например при адсорбции органических веществ, дает количественное совпадение с опытом при расчете емкости, если считать, что расстояние между обкладками равно размеру органической молекулы, а диэлектрическая проницаемость двойного слоя равна диэлектрической проницаемости органического вещества. [22]
Уравнение ( 25) позволяет в первом приближении объяснить форму электрокапиллярных кривых, полученных Гун [15 - 17], а также Батлером и Окрентом [34] в растворах, содержащих добавки органических соединений различных типов. [23]
Природа аниона обусловливает как назначение потенциала электрокапиллярного нуля, так и форму электрокапиллярной кривой в неводных растворителях, с чем и связано различное влияние неводных растворителей на кислородные максимумы в присутствии различных анионов. [24]
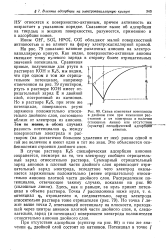 |
Схема изменения потенциала в двойном слое при изменении расстояния х от электрода и наличии ( сплошные линии или отсутствии ( пунктир специфической адсорбЩЙ анионов. [25] |
НРО, СОз обладают малой поверхностной активностью и не влияют на форму электрокапиллярной кривой. [26]
Природа аниона влияет как на потенциал электрокапиллярного нуля, так и на форму электрокапиллярной кривой в неводных растворах, что и обусловливает различное влияние неводных растворителей на кислородные максимумы в присутствии различных анионов. [27]
Поэтому в дальнейшем для описания влияния совместной адсорбции двух органических веществ на форму электрокапиллярной кривой [35] Батлером и Окрентом [36] была развита теория, использующая уравнение Шишковского с поправкой, аналогичной поправке Фрумкина [20], на аттракционное взаимодействие между адсорбированными частицами. В то же время полученные экспериментальные данные для смесей натриевых солей коричной и о-толуиловой кислот не согласуются с теорией, причем Аатеор Ааэксп. Это расхождение было объяснено авторами [36] влиянием электрических зарядов адсорбированных ионов, препятствующих дальнейшей адсорбции ионов того же знака. [28]
На основании графиков и численных значений е, о установить, чем вызвано изменение формы электрокапиллярной кривой. [29]
На основании графиков и численных значений е, а установить, чем вызвано изменение формы электрокапиллярной кривой. [30]
Страницы: 1 2 3 4 5