Форма - электрокапиллярная кривая
Cтраница 4
На основании графика, на котором построены зависимости о - Е для всех изученных растворов, делают заключение о влиянии адсорбции поверхностно-активных веществ на форму электрокапиллярных кривых. [46]
Поскольку строение двойного электрического слоя зависит от концентрации электролита и присутствия в нем поверхностно активных веществ, они будут существенно влиять на характер и форму электрокапиллярной кривой. [47]
В этом случае эффект органических веществ должен был бы проявляться лишь в очень узкой области потенциалов, непосредственно примыкающих к максимуму электрокапиллярной кривой. В действительности, изменение формы электрокапиллярной кривой под действием органических веществ наблюдается даже при потенциалах, удаленных на 0 5 - 0 8 в в обе стороны от потенциала максимума электрокапиллярной кривой. Это указывает на проявление специфических сил. Термин специфически адсорбирующиеся частицы, введенный ранее, отражает, таким образом, то обстоятельство, что поведение подобных частиц на границе ртуть - раствор не может быть обусловлено только силами электростатического происхождения. [48]
 |
Изменение заряда поверхности. [49] |
По достижении достаточно положительных потенциалов эффект этих катионов исчезает. Присутствие амилового спирта изменяет форму электрокапиллярной кривой главным образом в области потенциалов, примыкающих к потенциалу максимума. [50]
По достижении достаточно положительных потенциалов эффект этих катионов исчезает. Присутствие амилового спирта изменяет форму электрокапиллярной кривой главным образом в области потенциалов, примыкающих к потенциалу максимума. С удалением в обе стороны от потенциала электрокапиллярного максимума эффект снижается и кривая, снятая с добавкой спирта, совпадает с кривой для чистого раствора. [51]
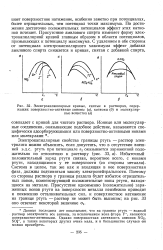 |
Электрокапиллярные кривые, снятые в растворах, содержащих поверхностно-активные анионы ( а, катионы ( б и молекулярные вещества ( б. [52] |
По достижении достаточно положительных потенциалов эффект этих катионов исчезает. Присутствие амилового спирта изменяет форму электрокапиллярной кривой главным образом в области потенциалов, примыкающих к потенциалу максимума. [53]
Уменьшение поляризации, очевидно, связано с анионной природой адсорбционной пленки адсорбатов и изменением - потенциала электрода. На такой характер адсорбции указывает и форма электрокапиллярных кривых. [54]
Более подробный анализ уравнения ( 489) показывает, что оно объясняет смещение потенциала максимума электрокапиллярной кривой в присутствии поверхностно-активных ионов и предсказывает направление смещения, вызываемое анионами и катионами. Однако оно не раскрывает характера влияния органических веществ на форму электрокапиллярных кривых. [55]
Измеряя высоту h при различных значениях потенциала и рассчитывая по уравнению ( 480) соответствующие ей величины сг, можно построить электрокапиллярную кривую. Для ряда разбавленных растворов ( например, H2SO4, КОН, KNO3, Na2SO4 и др.) форма электрокапиллярной кривой почти не зависит от природы электролита и близка к параболе. Максимум на кривой наблюдается при этом примерно при одном и том же значении потенциала, лежащем между - 0 19 и - 021 в по водородной шкале. В то же время электрокапиллярные кривые, полученные в растворах других электролитов, а также в присутствии большинства органических неионизированных веществ, сильно отличаются по своей форме от параболы. Они менее симметричны, с иным положением максимума. [56]
Измеряя высоту h при различных значениях потенциала и рассчитывая по уравнению ( Х-6) соответствующие ей величины 0, можно построить электрокапиллярную кривую. Для ряда разбавленных растворов ( например, H2SO4, КОН, KNCh, Na2SO4 и др.) форма электрокапиллярной кривой почти не зависит от природы электролита и близка к параболе. Максимум на кривой наблюдается при этом примерно при одном и том же значении потенциала, лежащем между - 0 19 и - 0 21 в по водородной шкале. В то же время электрокапиллярные кривые, полученные в растворах других электролитов, а также в присутствии большинства органических неионизированных веществ, сильно отличаются по своей форме от параболы. [57]
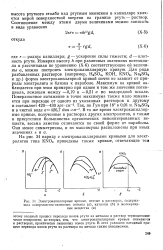 |
Электрокапиллярные кривые, снятые в растворах, содержащих поверхностно-активные. анионы ( я, катионы ( б и молекулярные вещества ( в. [58] |
Измеряя высоту h при различных значениях потенциала и рассчитывая по уравнению ( Х-6) соответствующие ей величины о, можно построить электрокапиллярную кривую. Для ряда разбавленных растворов ( например, H2SO4, КОН, KNO3, Na2SO и др.) форма электрокапиллярной кривой почти не зависит от природы электролита и близка к параболе. Максимум на кривой наблюдается при этом примерно при одном и том же значении потенциала, лежащем между - 0 19 и - 0.21 в по водородной шкале. Поверхностное натяжение в точке максимума также мало изменяется при переходе от одного из указанных растворов к другому и составляет 420 - 430 эрг-см-2. В то же время электрокапиллярные кривые, полученные в растворах других электролитов, а также в присутствии большинства органических неионизированных веществ, весьма заметно отличаются по своей форме от параболы. [59]
 |
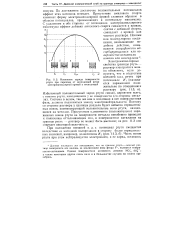
Капиллярный электрометр и электроизмерительная схема для снятия электрокапиллярных кривых. [60] |
Страницы: 1 2 3 4 5