Восстановленная форма - вещество
Cтраница 2
Когда в результате работы элемента окислитель восстановится, а восстановитель окислится и наступит равновесие между окисленной и восстановленной формой веществ, участвующих в реакции, или же просто будет нацело израсходован ( окислен) один из электродов, элемент перестанет работать. Вещества, могущие в нем реагировать, будут исчерпаны. [16]
Из этого уравнения можно сделать важный вывод: величина диффузионного тока пропорциональна разности соответствующих концентраций частиц восстановленной формы вещества. [17]
В большинстве случаев такими ионами являются ионы комплексообразователей, способных вступать во взаимоде-йствие с окисленной или восстановленной формой вещества. [18]
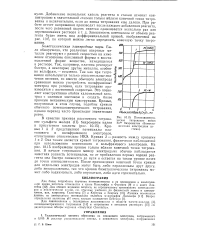 |
Потенциометри-ческое титрование ионов Fe2 бихроматом ( биметаллическая электродная система. [19] |
Было обнаружено, что различные инертные металлы реагируют с разной скоростью на изменение отношения окисленной формы к восстановленной форме вещества, находящегося в растворе. Так, например, платина реагирует быстро, а некоторые другие металлы, особен - f но вольфрам, - медленно. Так как при титро - ван ии используются только относительные зна - чения величин, то вместо обычного электрода § сравнения можно употреблять вольфрамовый электрод при условии, если титрование производится с постоянной скоростью. Это позволяет конструктивно обойти каломельный электрод с соляным мостиком и создать более прочную механическую конструкцию. Кривые, полученные в этом случае, подобны кривым обычного потенциометрического титрования, однако переход часто происходит значительно резче. [20]
Окисленная форма вещества с большим потенциалом является окислителем для восстановленных форм с более низким потенциалом, и наоборот, восстановленная форма вещества является восстановителем для окисленных форм с более высоким окислительным потенциалом. [21]
Окисленная форма вещества с большим потенциалом является окислителем для восстановленных форм с более низким потенциалом, и наоборот, восстановленная форма вещества является восстановителем для окисленных форм с более высоким окислитель ным потенциалом. [22]
Таким образом, стандартная плотность тока обмена i - это плотность тока обмена при стандартном потенциале, когда концентрации окисленной и восстановленной формы вещества равны единице. [23]
Окислительно-восстановительный электрод представляет собой пластинку из инертного металла ( Pt или Аи), погруженную в раствор, содержащий окисленную и восстановленную форму веществ. [24]
Окисленная форма вещества с большим потенциалом является окислителем для восстановленных форм с более низким потенциалом, и, наоборот, восстановленная форма вещества является восстановителем для окисленных форм с более высоким потенциалом. Таким образом, пользуясь стандартным потенциалом, можно определить, в каком направлении пойдет реакция, и рассчитать ее окислительно-восстановительный потенциал, величина которого равна разности потенциалов окислителя и восстановителя. [25]
В других случаях металл электрода не претерпевает изменений в ходе электродного процесса, а участвует лишь в передаче электронов от восстановленной формы вещества к его окисленной форме. [26]
Физический смысл этого равенства состоит в том, что мы вправе принять величину диффузионного тока пропорциональной разности соответствующих концентраций частиц восстановленной формы вещества. [27]
Каждая окислительно-восстановительная система также характеризуется определенным значением потенциала, который возникает на благородном металле, погруженном в раствор, содержащий окисленную и восстановленную форму вещества. [28]
R - газовая постоянная; Т - температура, К; аок - активность окисленной формы вещества; авосст - активность восстановленной формы вещества; п - число электронов, участвующих в реакции; F - число Фарадея. [29]
Сокисл и СВОсст - концентрации окисленной и восстановленной формы вещества; / Окисл - коэффициент активности окисленной формы вещества; fBoCCT - коэффициент восстановленной формы вещества; / ВОСст - коэффициент активности восстановленной формы вещества. [30]
Страницы: 1 2 3 4