Кислотная форма - индикатор
Cтраница 1
Кислотная форма индикатора имеет желтую окраску, а щелочная - красную. [1]
Кислотной формой индикатора называют форму, которая преобладает в кислотных растворах, а основной формой - ту, которая существует в основных ( щелочных) растворах. В некотором промежутке значений рН в растворе может одновременно находиться в равновесии некоторое количество обеих форм индикатора, вследствие чего возникает переходная окраска индикатора. Область значений рН, в которой совершается переход одной формы индикатора в другую и отмечается изменение окраски индикатора - это интервал рН перехода окраски индикатора, или просто интервал перехода индикатора. [2]
Принято называть кислотной формой индикатора ту, цвет которой преобладает в кислых средах, и основной формой - ту, цвет которой преобладает в щелочных средах. [3]
Принято называть кислотной формой индикатора ту, цвет которой преобладает в кислых средах, и основной - ту, цвет которой преобладает в щелочных средах. [4]
Здесь Тпдд - кислотная форма индикатора, способная отдавать протон; IndB - основная форма индикатора, способная присоединять протон. [5]
АН ] - концентрация кислотной формы индикатора, [ А - ] - концентрация основной формы. [6]
Окраска недиссоциированной молекулы HR ( кислотная форма индикатора) отличается от окраски аниона R - ( солевая форма) этой кислоты. [7]
Окраска в первой колбочке соответствует окраске кислотной формы индикатора, в третьей - окраске щелочной формы, окраска во второй колбочке соответствует цвету индикатора в зоне перемены окраски. [8]
При рН4 2 раствор имеет розовую окраску кислотной формы индикатора, а при рН6 2 - желтую окраску щелочной формы. Внутри указанного интервала окраска постепенно меняется от розовой к желтой. Молекула метилового красного является амфотерной, так как она содержит наряду с аминогруппой также и карбоксильную группу. [9]
Конец титрования определяют по моменту исчезновения окраски кислотной формы индикатора. Использование индикаторов с другими значениями рКа позволяет определить концентрацию кислотных центров различной силы. В качестве растворителя вместо, бензола можно использовать изооктан или четыреххлорис-тый углерод, а для титрования - ( бензиламин. [10]
В кислой среде равновесие смещено в сторону кислотной формы индикатора, раствор принимает окраску этой формы, а в щелочной среде окраска раствора соответствует окраске основной формы индикатора. [11]
При рН 3 1 раствор имеет розовую окраску кислотной формы индикатора, при рН 4 4 - желтую окраску щелочной формы. Внутри интервала окраска постепенно переходит из розовой в желтую. [12]
При рН 4 2 раствор имеет розовую окраску кислотной формы индикатора, а при рН 6 2 - желтую окраску щелочной формы. Внутри указанного интервала окраска постепенно меняется от розовой к желтой. Метиловый красный амфотерен, так как его молекула содержит наряду с аминогруппой также и карбоксильную группу. [13]
При рН 3 1 раствор имеет розовую окраску кислотной формы индикатора. [14]
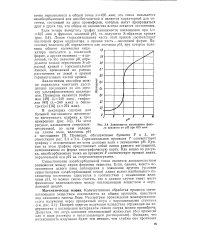 |
Зависимость поглощения фенола красного от рН при 615 ммк. [15] |
Страницы: 1 2 3