Диссоциация - угольная кислота
Cтраница 3
Вследствие сорбции ионов 11 значение рН воды возрастает и увеличивается диссоциация угольной кислоты. Эти реакции протекают не полностью, и концентрация бикарбонат-иона остается меньшей, чем исходная его концентрация. Поэтому фильтрат имеет небольшую щелочность. Однако величина этой щелочности изменяется во время фильтрования. Сначала наблюдается ее понижение, а к концу фильтроцикла она вновь увеличивается. [31]
Формулы выведены путем совместного решения уравнений первой и второй ступеней диссоциации угольной кислоты, ионного произведения воды и электронейтральности раствора, содержащего соединения угольной кислоты. [32]
Ион [ СОз2 - ] входит в уравнение второй константы диссоциации угольной кислоты, поэтому для решения воспользуемся ею. [33]
Формулы выведены путем совместного решения уравнений первой и второй ступеней диссоциации угольной кислоты, ионного произведения воды и электронейтральности раствора, содержащего соединения угольной кислоты. [34]
Ион [ СО3 - ] входит в уравнение второй константы диссоциации угольной кислоты, поэтому для решения воспользуемся ею. [35]
От прибавления к раствору - какой-либо сильной кислоты тгочти полностью подавляется диссоциация угольной кислоты и по первой ступени. Точио так же при Прибавлении водородных ионов к какому-нибудь карбонату образуется двуокись углерода; это происходит даже при прибавлении уксусной кислоты, и углекислый газ может быть легко полностью выделен при агревании. Единственными кислотами, не разлагающими карбонатов1, являются цианистоводородная, сернистоводородная и борная. [36]
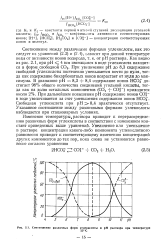 |
Соотношение различных форм углекислоты в рН раствора при температуре. [37] |
ЛЧ и / О, - константы первой и второй ступеней диссоциации угольной кислоты; / H, / нсо и / со - коэффициенты активности соответствующих ионов; [ Н ], [ HCCJJ ], [ Н2СО3 ] и [ СО1 - ] - концентрации соответствующих ионов и молекул. [38]
Коэффициенты / Ci и Кг являются константами первой и второй ступеней диссоциации угольной кислоты. [39]
Харнед и Боннер исследовали влияние хлорида натрия на константу первой ступени диссоциации угольной кислоты. Они установили, что в одномолярном растворе при 25 С значение К [ составляет 11 3 10 - 7 по сравнению с 4 45 - 10 - 7 в чистой воде. [40]
Скорость установления равновесия между СО2 и Н2СО3, а также продуктами диссоциации угольной кислоты при переходе С02 в воду мала, но измерима. Поэтому можно при помощи аналитических методов различить угольную кислоту НзСОз и сла-йогидратированный СО2 ( гидр. Эта низкая скорость процессов имеет большое значение в биологической, аналитической и промышленной химии. [41]
Эта зависимость показывает, что, несмотря на малое значение константы диссоциации угольной кислоты, диссоциацией воды можно пренебречь. [42]
Другой формой содержания угольной кислоты в воде являются гидрокарбонаты, образующиеся при диссоциации угольной кислоты по 1 - й ступени: Н2СО3 Н НСОГ. [43]
В первом случае изменение рН в процессе подщелачивания воды связано с первой ступенью диссоциации угольной кислоты. Во втором случае стабильность воды наступает при рН 8 4, поэтому вслед за первой здесь наступает и вторая ступень диссоциации. [44]
В первом случае изменение рН в процессе подщелачивания воды связано с первой ступенью диссоциации угольной кислоты. Во втором случае стабильность воды наступает при рН8 4, поэтому вслед за первой наступает вторая ступень диссоциации. [45]
Страницы: 1 2 3 4