Диссоциация - возбужденная молекула
Cтраница 3
Возбужденная молекула 2-нафтола является более сильной кислотой, чем невозбужденная, потому диссоциация возбужденной молекулы успешно конкурирует с флуоресценцией и безызлуча-тельными процессами деградации энергии электронного возбуждения. Это приводит к тому, что в спектре флуоресценции 2-яаф-тола даже в кислых растворах отчетливо видны две полосы. Более коротковолновая полоса соответствует флуоресценции недиссоциированного 2-нафтола, более длинноволновая - флуоресценции 2-нафтолят-аниона, образовавшегося при диссоциации возбужденной молекулы 2-нафтола. Увеличение концентрации ионов водорода в растворе подавляет диссоциацию возбужденного 2-нафтола. В спектрах флуоресценции это проявляется как увеличение интенсивности флуоресценции недиссоциированного 2-нафтола и уменьшении интенсивности флуоресценции 2-нафтолят-аниона. [31]
Возбуждение молекулы светом не обязательно приводит к химическому изменению вещества. Химические изменения возникают в результате процессов двух типов. Если переходы приводят к состоянию отталкивания со временем жизни меньше, чем период одного колебания, происходит диссоциация возбужденных молекул. В возбужденном или основном состоянии молекула может обладать колебательной энергией, достаточной, чтобы вызвать ее диссоциацию. Обычно разрываются те связи, которые ответственны за поглощение света. Химическая реакция может быть результатом межмолекулярного тушения возбужденной молекулы другой инородной молекулой. Процесс является первичным, основанным на взаимодействии тушителя и возбужденной молекулы. Возможен также вторичный процесс, который заключается в передаче энергии от возбуждения молекулы тушителю путем неупругого соударения, приводящего к их взаимодействию. Возбужденную молекулу, которая при этом переходит в основное состояние, часто называют фотосенсибилизатором. [32]
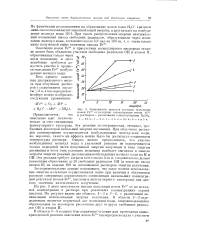 |
Зависимость выходов реакции окисления. [33] |
Эта реакция экзотермическая, очевидно, требующая некоторой небольшой энергии активации. При облучении растворов активирование осуществляется возбужденными молекулами воды, но, вероятно, такого же эффекта можно было бы достигнуть повышением температуры раствора. Однако можно предположить, что участие возбужденных молекул воды в указанной реакции не ограничивается только передачей части полученной энергии излучения в виде энергии активации и что в этих условиях возможна наиболее выгодная в смысле затраты энергии реакция диссоциации возбужденных молекул воды на Н и ОН. Эта реакция требует затраты всего около 5 эв и, следовательно, делает возможным образование до 20 свободных радикалов ОН ( и такое же число атомов Н) на каждые 100 эв поглощенной раствором энергии излучения. [34]
Значения kzlk могут быть получены из наклонов прямых 1 / Фд в опытах при данных температурах и длине волны; kz принимается равной Z2, и отсюда можно вычислить AJ. Удовлетворительное согласие данных по фотолизу кетена, полученных в опытах при 3660, 3340 и 3130 А, найдено Портером и Кеннеди [966] с использованием соотношения ( 6 - 66) для описания изменения &i в зависимости от энергии поглощенного кванта. В какой-то степени это совпадение, однако, можно считать случайным, поскольку большинство параметров в уравнении ( 6 - 66) были выбраны произвольно. Действительная диссоциация возбужденной молекулы должна протекать по гораздо более сложной схеме; Портер и Коннели рассматривают некоторые усложнения реального процесса. [35]
Диссоциация молекулы на два радикала в конденсированной фазе менее вероятна, чем в газовой. Образующиеся радикалы могут избежать быстрой рекомбинации только в том случае, если хотя бы один из них покинет место своего образования. Обладая в момент образования избыточной кинетической энергией, радикалы в газовой фазе быстро расходятся. В конденсированной же фазе энергия радикалов быстро передается окружающим молекулам, в результате радикалы, не успевая разойтись, рекомбинируют. Эффект клетки, по-видимому, играет меньшую роль при диссоциации молекулярных катионов, свободных радикалов и других частиц с неспаренным электроном. При разрыве связи в парамагнитной частице образуется не пара радикалов, а радикал и молекула, которые, естественно, не могут рекомбинировать. Эффект клетки не играет большой роли также в случае диссоциации возбужденной молекулы с разрывом связи С - Н, так как атомы водорода легко диффундируют в большинстве твердых матриц при низкой температуре. [36]
Страницы: 1 2 3