Диссоциация - водяной пар
Cтраница 1
Диссоциация водяного пара в газовой фазе зоны сварки способствует повышению содержания в сварочной ванне водорода и кислорода. [1]
Диссоциация водяных паров в зависимости от условий протекания реакции может создать для жидкого металла окислительную или восстановительную атмосферу. [2]
Реакция диссоциации водяного пара, обратная процессу горе-ия водорода, может протекать в той или иной мере в горячем пламени водорода, реагирующего с кислородом. [3]
Степень диссоциации водяного пара или углекислоты увеличивается с уменьшением давления или увеличением объема. [4]
При изучении диссоциации водяного пара при высоких температурах на водород и кислород было найдено, что температурная зависимость константы К. [5]
Водород, образующийся при диссоциации водяного пара или в результате реакций водяного пара с металлической поверхностью, может также вступать во взаимодействие с металлом, образуя или твердые растворы, или гидриды с такими металлами, как Ti; Zr; V; Nb. Аналогично нитридам, гидриды накапливаются у этих металлов также главным образом в поверхностных слоях, толщина которых определяется скоростью диффузии. Поглощение водорода металлами приводит к падению пластических свойств ( водородной хрупкости), так как водород, проникая в металл по месту кристаллических нарушений - дислокаций, тормозит их возможные перемещения. [6]
Таким образом, степень диссоциации водяного пара при температуре 2000 примерно втрое меньше степени диссоциации двуокиси углерода. [7]
С увеличением температуры степень диссоциации водяных паров увеличивается и при 5000 К приближается к единице. [8]
Таким образом, степень диссоциации водяного пара при температуре 2000 примерно втрое меньше степени диссоциации двуокиси углерода. [9]
 |
Тепловой эффект реакции. [10] |
Рассмотрим, например, диссоциацию водяного пара. [11]
Возможность поглощения водорода обусловлена диссоциацией водяных паров, содержащихся в воздухе. [13]
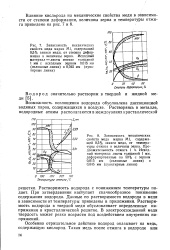
На рис. 24 дана кривая диссоциации водяного пара. Числа для низких температур получены конечно не прямыми методами. Увеличение давления эту диссоциацию подавляет. [14]
Эта величина определяется из уравнения диссоциации водяного пара на кислород и водород. [15]
Страницы: 1 2 3 4