Диссоциация - водяной пар
Cтраница 2
ОН и перекиси водорода Н2О2 При диссоциации водяных паров одним из решающих обстоятельств является изменение числа газовых молекул и связанная с этим зависимость состояния равновесия от общего давления газовой системы. Мы прилагаем здесь график, показывающий характер этой зависимости для функции AFH. [16]
Однако при температурах выше 2000 К диссоциация водяного пара значительна. [17]
Диссоциация двуокиси углерода происходит в большей степени, чем диссоциация водяного пара. [18]
Парциальные равновесные давления могут быть подсчитаны из значений степеней диссоциации водяного пара. [19]
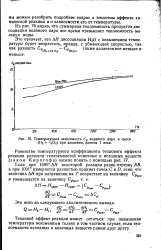 |
Температурная зависимость Ср водяного пара и смеси ( Н2 V2O2 при давлении, равном 1 атм. [20] |
Из рис. 76 видно, что суммарная теплоемкость продуктов диссоциации водяного пара все время превышает теплоемкость молекул воды. [21]
До какого значения надо повысить давление, чтобы степень диссоциации водяного пара уменьшилась вдвое, если исходное давление было равно 0 5 бар. [22]
Калориметрическая температура горения tK - температура, которая определяется без учета диссоциации водяных паров и диоксида углерода, но с учетом фактической начальной температуры газа и воздуха. Она отличается от жаропроизводительности 1 тем, что температура газа и воздуха, а также коэффициент избытка воздуха а принимаются по их действительным значениям. [23]
Уменьшение константы / Ср показывает, что с повышением температуры степень диссоциации водяных паров увеличивается и в равновесной газовой смеси возрастает содержание водорода и кислорода. Степенью диссоциации х будем считать часть каждой граммолекулы водяных паров, которые распадаются, образуя равновесную газовую смесь. [24]
Примерами эндотермических реакций могут служить реакции, обратные указанным выше; так, диссоциация водяного пара на водород и кислород, происходящая при высоких температурах, сопровождается поглощением теплоты. [25]
По известному значению константы равновесия реакции из этого уравнения может быть вычислена степень диссоциация водяного пара при данных условиях. [26]
Примерами эндотермических реакций могут служить реакции, обратные указанным выше; так, диссоциация водяного пара на водород и кислород, происходящая при высоких температурах, сопровождается поглощением теплоты. [27]
По известному значению константы равновесия реакции ЕЗ этого уравнения может быть вычислена степень диссоциации водяного пара при данных условиях. [28]
Изменение содержания влаги в дутье доменных печей нарушает постоянство условий производства, так как на диссоциацию водяного пара расходуется значительное количество тепла. Расчеты показывают, что изменение влажности дутья на 1 10 - 3 кг / м3 вызывает изменение температуры в фурменной зоне на 9 С. Кроме того, диссоциация влаги на кислород и водород изменяет восстановительную способность горновых газов и условия горения кокса у фурм. [29]
 |
Химические постоянные различных газов. [30] |
Страницы: 1 2 3 4