Диссоциация - водяной пар
Cтраница 4
При определении термодинамических свойств перегретого водяного пара в области весьма высоких давлений и температур до р 1000 кг / см2 и t 1000 С предположено, что установленные опытом законы в пределах исследуемых давлений до р - 500 am и t 600 С распространяются и на области более высоких температур, до таких значений температуры, при которых состояние пара претерпевает или фазовые изменения или имеет место влияние диссоциации водяного пара на кислород и водород. Нижней границей значений температур, при которых в области весьма высоких давлений заметно влияние фазовых изменений, принята температура t 550 С. Верхней границей значений температур, за которой заметно влияние диссоциации при малых и средних давлениях пара, принята температура t 1000 С. [46]
Вероятность реакции, полученная в этой работе для реакции С Н20 СО Н2, примерно в 102 раз больше тех, которые определены в исследованиях при низких давлениях на нитях из того же пиролитического углерода. Предполагается, что это есть результат диссоциации водяного пара в горячих продуктах горения, при которой образуются активные радикалы ОН. [47]
 |
Характеристики процесса диссоциации воды. [48] |
Теоретический состав диссоциированного водяного пара устанавливается в процессе с высокой скоростью. Рассчитано, что 90 % - ная диссоциация водяного пара достигается за 10 - 2; 10 - 3 и 10 - 4 с соответственно при 2200, 2500, 3000 К. [49]
Еще Аррениус показал, что при 300 С кислотные свойства воды и кремнекислоты аналогичны. Рассчитано [61-63], что ниже 4200 С диссоциация водяного пара протекает преимущественно по уравнению: H2U Н2 / 2 Ог - По другим данным, возникают гидроксил и кислород в виде свободных радикалов, которые весьма активны. [50]
В качестве конечного шага проверяются равновесия, которые могли не учитываться при составлении уравнений. В данном случае наиболее вероятной может быть диссоциация водяного пара на водород и кислород. Если, основываясь па равновесных величинах, найденных выше для пара и водорода, действительно доказано, что количество кислорода незначительно, то процедура является законной. Однако если количество кислорода сравнимо с количествами других второстепенных компонентов, то уравнения (2.2) - (2.4) должны быть переписаны с включением этого компонента и процесс должен быть снова повторен. [51]
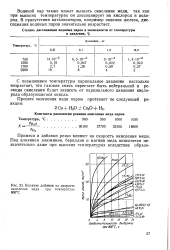 |
Влияние добавок на скорость окисления меди при температуре 800 С. [52] |
Водяной пар также может вызвать окисление меди, так как при высоких температурах он диссоциирует на кислород и водород. В присутствии катализаторов, например окислов железа, диссоциация водяных паров значительно возрастает. [53]
Наиболее тщательные исследования гомогенных газовых реакций, как, например, диссоциации водяного пара и углекислого газа, были выполнены на раскаленной платиновой нити. [54]
В 1931 - 1932 гг. Мерцаловым была написана для Технической энциклопедии статья Термодинамика, в которой была обобщена его многолетняя работа по этой дисциплине. В 1944 г. Мерцалов заканчивает небольшую, но весьма интересную научную работу О диссоциации водяного пара. Здесь автор на основании общих дифференциальных уравнений термодинамики выводит формулу для подсчета состава смеси при диссоциации водяного пара в зависимости от давления и температуры и сравнивает результаты вычисления по этой формуле с опытными данными. [55]
Здесь для качественного рассмотрения может быть использован упоминавшийся в предыдущем параграфе принцип Ле-Шателье. Например, повышение температуры равновесной смеси газов Н2, СЬ, Н2О приводит к увеличению диссоциации водяного пара, сопровождающейся поглощением тепла. Однако принцип Ле-Шателье не имеет общего характера. Он был предложен как аксиома, не опирающаяся на какой-либо определенный физический закон. Применение принципа Ле-Шателье в некоторых случаях может привести к ошибочным утверждениям. [56]
Ведущая роль радикалов Н и ОН характерна для цепного механизма горения всех углеводородов. Даже оксид углерода СО, в составе которого нет атомов водорода, по современным представлениям сгорает с участием радикалов, образующихся при диссоциации водяного пара. [57]
Страницы: 1 2 3 4