Диссоциация - ионная пара
Cтраница 1
Диссоциация полученной ионной пары на конечные продукты про-толитического равновесия В и SH2 определяется прежде всего полярностью растворителя, мерой которой является его диэлектрическая постоянная D. [1]
Рассмотрим снова задачу о диссоциации ионной пары. [2]
Альтернативой этому является процесс диссоциации ионной пары ( характеризующийся константой скорости k), приводящий к симметрично сольватированному карбониевому иону и, следовательно, к образованию рацемического продукта. Однако в настоящее время известно, что явление ассоциации ионов гораздо сложнее, чем предполагает изложенная выше гипотеза. В частности, рацемизация может происходить раньше, чем начнется атака растворителя ( разд. В случае когда в реакции замещения участвует ионный нуклеофильный агент, как карбониевый ион, так и нуклеофильный агент могут существовать в виде ионных пар. В подобном случае можно считать [1249], что реакция протекает с промежуточным образованием ионных квадруплетов. [3]
Такая схема реакций предполагает, что скорость диссоциации ионной пары ( H20) 5Cr3 SCN - меньше, чем скорость ее перегруппировки, образования N-связанного изомера или реакции аквотации. Только что описанная изомеризация ( H20) 5Cr - SCN2 является спонтанной. [4]
Так как катионная полимеризация связана с образованием и диссоциацией ионной пары, то на скорость процесса оказывает влияние диэлектрическая проницаемость среды. Повышение диэлектрической проницаемости существенно ускоряет - процесс, но мало сказывается на молекулярной массе полимера. В сравнении с радикальной, катионная полимеризация характеризуется низкой энергией активации ( 60 кДж / моль), поэтому она протекает с высокой скоростью, которая снижается с повышением температуры. [5]
Так как катионная полимеризация связана с образованием и диссоциацией ионной пары, то на скорость процесса оказывает влияние диэлектрическая проницаемость среды. Повышение диэлектрической проницаемости существенно ускоряет процесс, но мало сказывается на молекулярной массе полимера. В сравнении с радикальной, катионная полимеризация характеризуется низкой энергией активации ( 60 кДж / моль), поэтому она протекает с высокой скоростью, которая снижается с повышением температуры. [6]
Легко видеть, что влияние сольватации сказывается и при образовании сольватированной пары, и при диссоциации ионной пары. [7]
Кинетическими исследованиями установлено, что именно ад-дукт А1СЬ с хлорангидридом кислоты в биполярной или ионной форме, а не ацил-катион, получающийся при диссоциации ионной пары, образует о-комплекс при реакции ароматического ацилирования. [8]
Этот опыт, проведенный в отсутствие источников протонов, дает мало сведений об истинном характере процесса рацемизации, который может протекать за счет либо диссоциации ионной пары, либо реакции перестройки ионной пары. В табл. 39 приведены соответствующие данные. [9]
Разница в величинах рКа для соединения XII и для иона трипропиламмония составляет примерно 8, а следовательно, протонирование должно происходить быстрее, чем диссоциация ионной пары. [10]
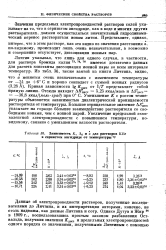 |
Зависимость К, Л0 и а для растворов КВг в сернистом ангидриде от температуры 7Р. [11] |
Личтин указывал, что лишь для одного случая, в частности, для раствора бромида калия 73 7 76 имеется достаточно данных для расчета константы диссоциации ионной пары во всем интервале температур. [12]
Свейн полагает, что первый порядок рацемизации в спиртовых или водных растворах обусловлен быстрым образованием иона карбония, сольватированного двумя молекулами растворителя, которое облегчается диссоциацией ионной пары в этих полярных растворителях и высокой концентрацией гидроксильных ионов. В водных растворах вследствие большого размера соль-ватной оболочки гидроксильного иона он не может достаточно сблизиться с центральным атомом углерода третичных галогени-дов, и при этих обстоятельствах гидроксильный ион не ускоряет таких реакций. [13]
 |
Общий механизм пзорацемизации. [14] |
Однако, поскольку обмен идет в некоторой степени и в отсутствие добавленных солей, этот факт свидетельствует о том, что частично обмен может происходить по механизму, включающему диссоциацию ионной пары. [15]
Страницы: 1 2 3