Диссоциация - растворитель
Cтраница 2
Наряду с описанными выше веществами существуют многочисленные соединения, которые в результате реакции с растворителем смещают равновесие диссоциации растворителя и тем самым вызывают повышение концентрации одного из ионов. Такие вещества называют ансольвосоединениями. [16]
Таким образом, это произведение не зависит от индивидуальных свойств сопряженной пары кислота - основание и является только функцией диссоциации растворителя. Из этой зависимости вытекают некоторые важные следствия. Если в растворителе с известным ионным произведением проходит реакция кислотной диссоциации, то, исходя из - значения ее константы диссоциации, легко вычислить константу диссоциации сопряженного основания. И наоборот, если известна константа диссоциации основания, то мы можем тут же рассчитать константу диссоциации сопряженной кислоты. Поэтому во многих современных руководствах в таблицах приводят не константы диссоциации кислот и независимо от них константы диссоциации оснований, а только константы кислотной диссоциации. [17]
Для вывода уравнения, характеризующего АОСН рассмотрим вновь реакцию обмена протона в вакууме и сопоставим ее с константой аутопро-толиза - реакций диссоциации растворителя в вакууме. [18]
Для вывода уравнения, характеризующего / Сдосн, рассмотрим вновь реакцию обмена протона в вакууме и сопоставим ее с константой аутопро-толиза-реакций диссоциации растворителя в вакууме. [19]
Изоионным раствором белка называется такой раствор, который, помимо растворенного белка, не содержит иных ионов, кроме тех, которые образовались в результате диссоциации растворителя. Например, если водный раствор белка пропустить через смешанную ионообменную колонку, все катионы и анионы, кроме массовых ионов белка, заменятся на ионы П и ОН, и образовавшийся раствор будет по определению изоионным. [20]
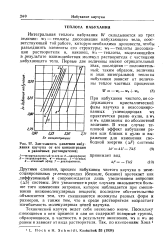 |
Зависимость давления набу - г. [21] |
Интегральная теплота набухания W складывается из трех величин: wi - теплоты диссоциации набухающего тела, соответствующей той работе, которую необходимо произвести, чтобы разъединить элементы его структуры; w - 2 - теплоты диссоциации растворителя и, наконец, wa - теплоты, выделяющейся В результате взаимодействия молекул растворителя с частицами набухающего тела. [22]
 |
Номограмма для определения рН растворов кислот или оснований в неводных растворителях, когда диссоциации электролита и растворителя соизмеримы. [23] |
Для определения рН растворов кислот и оснований в неводных протоли-тических растворителях используют номограммы, приведенные на рис. 2.4 и 2.5. Номограмму ( рис. 2.4) применяют для очень слабых в данном растворителе электролитов, когда их диссоциация соизмерима с диссоциацией растворителя. [24]
В экспериментально определенное число переноса, рассчитанное по формуле ( 17), следует ввести поправку на электропроводность растворителя [32], так как общий ток i имеет две составляющих: г г эл i, где i - ток, переносимый ионами исследуемого электролита, и i - ток, переносимый ионами, образующимися при диссоциации растворителя и его примесей. [25]
При этом значительно усиливается диссоциация растворителя вследствие влияния поля на диссоциацию. При этом обычно нужна только одна установка и используются всего несколько миллилитров раствора; метод применим к тому же для большинства растворителей. [26]
Ионы водорода в водном растворе сильной кислоты поступают из двух источников: 1) в результате реакции взаимодействия растворенной кислоты с водой и 2) в результате диссоциации самой воды. В не слишком разбавленных растворах вклад реакции взаимодействия растворенного вещества с растворителем в суммарную кислотность значительно превышает вклад диссоциации растворителя. [27]
Приведенный способ расчета ошибки титрования правилен в большинстве встречаемых на практике случаев. Однако если растворы очень разбавлены или конечная точка существенно отличается от рН 7 0, то необходимо проводить более точные вычисления, учитывая как диссоциацию неоттитрованной части кислоты, так и влияние ионов Н30 и ОН, получающихся при диссоциации растворителя. Поэтому необходимо в числителе уравнения ( 10) уменьшить концентрацию НА на неоттитрованную часть, которая диссоциировала. [28]
 |
Твердость по Роквеллу.| Температура тепловой деформации DGEBA, отвержденного высокоцианоэтилированным1 амином [ Л. 2 - 7 ]. [29] |
В композициях, используемых для покрытий, применение простых смесей, кетонов с аминами предпочтительнее применения конденсатов вследствие того, что в этом случае при сохранении всех преимуществ конденсатов исключается необходимость отвода воды, образующейся в процессе реакции. Например, обычное смешивание DETA с метилэтилкетоном дает комплекс, обладающий низкой вязкостью, который, будучи введен в DGEBA, обеспечивает время жизни около 6 ч и быстрое отверждение с образованием пленки толщиной около 0 12 мм, при этом происходит диссоциация растворителя и его испарение. [30]
Страницы: 1 2 3