Диссоциация - связь
Cтраница 3
Энергия диссоциации связи С-С этана CHS - CHS равна, согласно табл. 18, 85 ккал / моль. Отсюда следует, что энергия ассоциации двух радикалов СН, на 74 ккал больше, чем энергия ассоциации двух радикалов ( СвН8) 3С ( Следует заметить, что эти цифры нельзя строго сопоставить, так как один из радикалов находится в газовой фазе, а другой - в растворе. [31]
Энергии диссоциации связей С - Н были получены в результате измерений методом электронного удара как непосредственно, так и косвенным путем. Энергия диссоциации D ( CH3 - Н) в метане была определена [191] путем измерения потенциала появления ионаСНз когда метан подавали в ионизационную камеру. [32]
Энергии диссоциации связи для связей С - Н и теплоты образования алкил-радикалов, которые были получены по методу электронного удара [193], приведены в табл. 37 вместе с теплотами образования углеводородов, на которых они основаны. [33]
Энергия диссоциации связи С - С этапа СН3 - СН3 равна, согласно табл. 18, 85 ккал / молъ. Отсюда следует, что энергия ассоциации двух радикалов СН3 - па 74 ккал больше, чем энергия ассоциации двух радикалов ( СбН5) 3С ( Следует заметить, что эти цифры нельзя строго сопоставить, так как один из радикалов находится в газовой фазе, а другой - в растворе. [34]
Энергия диссоциации связи находится в зависимости от устойчивости радикала, образующегося в результате диссоциации. Как известно, устойчивость радикала определяется его способностью к делокализации одиночного, неспаренного электрона. Эта способность увеличивается при введении как электронодонор-ных, так и электроноакцепторных заместителей. Известна феноменальная устойчивость свободных триарилметильных радикалов, существующих в растворе без доступа кислорода в равновесии со своим димером неопределенно долгое время. Бензильный и аллильный радикалы относятся к короткоживущим радикалам, однако для их образования требуется значительно меньше энергии ( см. табл. 5), чем для образования других алкильных или арильных радикалов, и, следовательно, при подходящих условиях гемолитический разрыв в первую очередь будут испытывать именно аллильные или соответственно бензильные С - Н - связи углеводородов. [35]
Энергия диссоциации связи равна энергии активации распада молекулы на радикалы, так как обратная реакция соединения радикалов идет с нулевой энергией активации. [36]
Энергия диссоциации связей С-С меньше, чем связей С - Н, Однако, в случае низших метановых углеводородов, ( этан, пропан) преобладающим является распад по С - Н связи, что объясняется более высокой вероятностью разрыва этих связей вследствие их большего числа и доступности атомов водорода атаке свободных радикалов. Наиболее термически устойчив метан. [37]
Теплоты диссоциации связи N-N, измеренные для ряда ди-арилацилгидразилов типа ( VI), доходят до 18 ккал, так что по величине они близки к теплоте диссоциации связи С-С в соединениях ряда гексаарилэтана ( стр. Однако следует отметить, что скорость диссоциации арилированных гидразинов и тетразанов гораздо меньше, чем в случае аналогичных гекса-рилэтанов. [38]
Энергия диссоциации связи N - N считается равной 21 ккал / моль ( см. гл. [39]
Энергия диссоциации связи N - N в молекуле 19 8 ккал / моль, средняя энергия диссоциации связи N - F 71 0 ккал / моль. [40]
Энергия диссоциации связи R-С в таком процессе ( который является реакцией, обратной стадии роста цепи в соответствующем процессе винильной полимеризации) очень мала и составляет всего около 20 ккал / моль. Это обусловлено тем, что разрыв связи сопровождается выигрышем энергии я-связи; исходный радикал насыщенный, тогда как один из продуктов реакции включает двойную связь. Мы не считаем рациональным описывать такое увеличение энергии я-связей как увеличение энергии резонанса. [41]
Энергия диссоциации связи С-N в 1-нитропропане составляет 55 9 ккал / моль. [42]
Энергия диссоциации связи С-N в динитрометане равна 53 9 ккал / моль. [43]
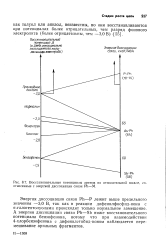 |
Восстановительные потенциалы аренов по относительной шкале, соотнесенные с энергией диссоциации связи Ph - М. [44] |
Энергия диссоциации связи Ph - Р лежит выше предельного значения - 3 0 В, так как в реакции дифенилфосфид-иона с я-галогентолуолами происходит только нормальное замещение. А энергия диссоциации связи Ph-Sb ниже восстановительного потенциала бензофенона, потому что при взаимодействии 4-хлорбензофенона с дифенилстибид-ионом наблюдается перемешивание арильных фрагментов. [45]
Страницы: 1 2 3 4