Функция - кислотность - гаммет
Cтраница 1
Функция кислотности Гаммета Я0 для SiO2 составляет от 4 до 6 8, окись алюминия также имеет очень слабые кислотные свойства ( Я0 - 4), а алюмосиликаты имеют Я0 - 8 2, их кислотность близка к кислотности серной кислоты, нанесенной на силикагель. С изменением соотношения SiO2: А12О3 в алюмосиликатах изменяется кислотность и по Бренстеду, и по Льюису. Кислотность по Льюису максимальна для чистой окиси алюминия и с увеличением содержания SiO2 уменьшается, для чистой двуокиси кремния они приблизительно равна нулю. [1]
Функция кислотности Гаммета позволяет распространить традиционную шкалу кислотности на ряд систем, хотя она все же не является универсальным способом определения кислотности, действительным для всех растворителей. Для установления шкалы Гаммета необходимо, чтобы применяемые индикаторы имели сходные механизмы кислотно-основной диссоциации, были одинаково сольватированы и не подвергались побочным, мешающим реакциям. Поэтому шкалу Гаммета и не удалось применить к растворителям с малой диэлектрической проницаемостью ( например, к безводной уксусной кислоте), так как реакция кислота - основание приводит в таких случаях к образованию ионных пар анион-катион, что не позволяет создать шкалу кислотности. Тем не менее, например, в водно-спиртовых растворах эта функция находит широкое применение. [2]
 |
Зависимость функции кислотности Я0 серной кислоты в смеси фенола и ацетона при 25 С. [3] |
Значения функции кислотности Гаммета, полученные индикаторным методом, зависят от содержания воды. [4]
Характер изменения функции кислотности Гаммета ( см. рис. 7) показывает, что активность серной кислоты в значительной степени зависит от содержания в ней воды и резко снижается с увеличением концентрации кислоты. Это особенно заметно в области высоких концентраций. Поскольку функция кислотности серной кислоты в растворе углеводородов намного больше, чем в воде, снижение активности катализатора при ал: илиро-вании будет в первую очередь определяться его разбавлением водой и в меньшей мере растворением в нем высокомолекулярных углеводородов - продуктов побочных реакций. [5]
Поскольку определение функции кислотности Гаммета связано с необходимостью отыскания большого набора кислотно-основных индикаторов с последовательно уменьшающейся основностью, а это для ряда сред так и не выполнено, то метод Стрелова выглядит предпочтительнее. Бейтс [58] уделяет значительное внимание функциям кислотности, поэтому мы затронем лишь один аспект проблемы единой шкалы кислотности, в котором интересные результаты были получены при использовании системы ферроцен - феррицений в качестве сравнительной системы. [6]
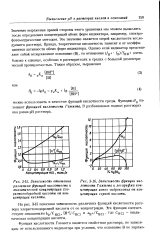 |
Зависимость отношения различных функций кислотности к аналитической концентрации хлористоводородной кислоты от концентрации кислоты. [7] |
Функцию Я0 называют функцией кислотности Гаммета. В разбавленных водных растворах она равна рН раствора. [8]
Значения ран совпали со значениями функции кислотности Гаммета Я0, что было интерпретировано [2] как экспериментальное доказательство гипотезы Гаммета о неизменности отношений коэффициентов активности ионизованной и неионизованной форм незаряженного основания при изменении кислотности среды. Мы в свое время воздержались от такого толкования, считая, что опытных данных еще недостаточно для такого категорического утверждения. [9]
Бейтс и Шварценбах подвергли критике функцию кислотности Гаммета и пришли к заключению, что значение Н0 существенно зависит от индивидуальных свойств используемого индикатора. [10]
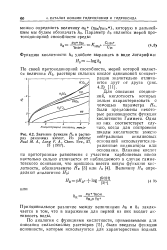 |
Значение функции Я0 в растворах различных кислот. Из работы. Paul M. A., Long F. A., Chem. Rev., 57, 13 ( 1957. [11] |
Яо, были предложены некоторые разновидности функции кислотности Гаммета. Одна из них соответствует случаю, когда для построения шкалы кислотности вместо нейтральных анилиновых оснований используются заряженные индикаторы или основания. [12]
Было установлено, что измеряемая индикаторным методом функция кислотности Гаммета для водных растворов сильных кислот представляет собой логарифм термодинамической активности протонов. В случае мономолекулярных процессов, катализируемых кислотами, истинная константа скорости не зависит от содержания воды в растворе. Предложены критерии для оценки реакционной способности веществ в бимолекулярных процессах, протекающих в водных растворах сильных кислот. [13]
Смит и Эллиот67, применяя в качестве индикаторов а-нафтол-бензоил и о-нитроанилин, вычислили функцию кислотности Гаммета h0 для разбавленных растворов ряда сильных кислот в ледяной уксусной кислоте. Это было интерпретировано как результат диссоциации ионной пары. [14]
При сравнении протонодонорлой активности растворов заданной концентрации кислоты в различных растворителях оказывается, что функция кислотности Гаммета тем выше, чем ниже основность растворителя. Например, раствор НС1 в бензоле имеет значительно большую кислотность, чем в воде. Определяется это тем, что С1 - значительно более слабое основание, чем вода. Таким же образом растворы серной кислоты в-уксусной обладают значительно большей прогонодоиорной активностью ( характеризуемой Я0), чем растворы такой же концентрации в воде. [15]
Страницы: 1 2 3 4