Функция - кислотность - гаммет
Cтраница 2
Химические свойства HF определяются двумя факторами: ярко выраженной кислотностью безводного HF ( для 100 % - го HF функция кислотности Гаммета Я0 - 10 2) и способностью к образованию комплексных соединений. [16]
Существенный вклад в теорию применения ЛССЭ к гетерогенному катализу вносит учет функции распределения каталитических центров по коррелирующему параметру, например по функции кислотности Гаммета. [17]
Химические свойства II F определяются в основном двумя факторами: ярко выраженной кислотностью безводного HF ( для 100 % - ного II F функция кислотности Гаммета Н - 10 2) и способностью к образованию комплексных соединении. Во многих случаях способность HF реагировать с тем или иным в-вом ограничивается образованием плотной пленки нерастворимого фторида. Так, Mg, Al, Zn, Cd, Fe н многие другие металлы не вытесняют водорода из безводной HF из-за образования пленки нерастворимого в IIF фторида металла. Характерной особенностью II F является способность интенсивно реагировать со многими силикатными материалами, в частности со стеклом. [18]
Редокс-функция кислотности, введенная Стреловым, представляет величину R0 ( H) ES - lg ( h - y Fec / y Fec), которая по своей структуре соответствует функции кислотности Гаммета Н0 ЕЕ; - lg ( h - y B / y BH), где if - нулевые коэффициенты активности [54] или эффект среды [58]; В - основная форма ( незаряженная) индикатора; ВН - кислотная форма, несущая положительный заряд. При нормировках у ] - - 1 в воде все эти функции стремятся к рН при переходе к чисто водным растворам. [19]
Однако в настоящее время имеются данные, что гипотеза Гаммета - Цукера в этом случае неприемлема [79], а недавно было показано, что дедейтерирование и детритирование толуола или бензола в серной кислоте не подчиняются точно функции кислотности Гаммета. Чогвилл и Ридд [84], изучая протодеиодирование n - иоданилина в водных растворах, также пришли к выводу, что медленный перенос протона от кислоты к ароматическому субстрату может быть стадией, определяющей скорость реакции. [20]
Установленный факт существования взаимосвязи между ctpyi турой растворов, с одной стороны, и кислотностью, с другой, также взаимной зависимости изменений этих характеристик pa ci вора при введении в него растворяемых веществ обосновывает во; можность использования функции кислотности Гаммета при ouei ке растворяющей способности различных кислот - важнейши растворителей неорганических веществ. Выявленная взаимосвяз этих двух важных характеристик раствора позволяет, изменяя oj ну из них, направленно изменять другую и тем самым направле; но смещать кислотно-основное равновесие, а следовательно, в oi ределенной степени управлять протеканием процесса. [21]
Мы можем сделать вывод, что хотя применение водного раствора минеральной кислоты позволяет получить чрезвычайно широкий спектр кислот-ностей, которые переходят постепенно в шкалу рН и могут быть использованы для размещения почти всех оснований на одной эмпирической калибровочной кривой, в функции кислотности Гаммета нет ничего универсального или абсолютного. [22]
Шкала Н0 является естественным продолжением шкалы рН в область концентрированных растворов кислот. Функция кислотности Гаммета позволяет с некоторым приближением характеризовать протонодонорную активность концентрированных кислот и растворов кислот в различных растворителях. При этом соотношение протонодонорной активности данного ряда кислот в различных растворителях приближенно сохраняется. [23]
Шкала кислотности Н0 является ценным критерием сравне-i ния не только основных органических соединений, но и силы ca-tj мих кислот. Так, функции кислотности Гаммета для некоторых суперкислот имеют следующие значения: хлорсульфоновая, кислота Нй - 12 8, фторсульфоновая кислота Н0 - 15 07, олеум ( при содержании серного ангидрида 75 % мол. [24]
Хлорметандисульфоновая, метантрисульфоновая [763] и фторсульфо-новая кислоты [627] в среде уксусной кислоты даже более сильные кислоты, чем хлорная, однако широкого применения они пока не нашли. На рис. 36 даны значения функции кислотности Гаммета Я о для сильных кислот в среде уксусной кислоты [625, 763] и графически показана зависимость этой функции от отрицательного логарифма концентрации кислоты СА. [25]
На рис. 7 показано изменение функции кислотности серной и фтористоводородной кислот в зависимости от их концентрации в воде. Как видно, при равных концентрациях функция кислотности Гаммета и, следовательнэ, активность серной кислоты гораздо выше соответствующих значений для фтористоводородной кислоты. [26]
Смысл показателя кислотности рН существенно изменяется в неводных средах и даже в водных растворах с высокой концентрацией электролита, В растворах с ионной силой выше 0 1 М использование величины рН в качестве меры кислотности уже неправомерно. Существуют и другие шкалы кислотности, например функция кислотности Гаммета, которая обсуждается ниже. [27]
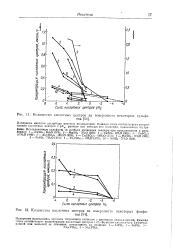 |
Количество кислотных центров на поверхности некоторых сульфатов.| Количество кислотных центров на поверхности некоторых фосфатов. [28] |
Каждая точка соответствует концентрации кислотных центров с Я0 ( функция кислотности Гаммета), равной или меньшей ее значения, показанного на графике. [29]
Ниже рассматривается ряд общих вопросов, необходимых для понимания кислотно-основных систем, а также некоторые кислотно-основные реакции, протекающие в трех наиболее типичных растворителях. В конце главы описаны методы измерения рН в смесях растворителей и функция кислотности Гаммета. [30]
Страницы: 1 2 3 4