Каталитическая функция
Cтраница 2
Этот факт подтверждает каталитическую функцию С02: при конденсации ацетил - SKoA с малонил - SKoA освобождается ровно столько же С02, сколько было использовано в ацетил - КоА - карбоксилазной реакции. [16]
Ряд кислот Льюиса выполняет каталитические функции, активируя не органический реагент, а протонную кислоту, представляющую собой сокатализатор. [17]
Иногда в реальных условиях активные каталитические функции выполняются лишь очень небольшой мольной долей катализатора. В гомогенном катализе довольно часто случается, что истинно каталитические частицы в действительности не являются гомогенными. [18]
Никотинамидные коферменты осуществляют свои каталитические функции переноса водорода как в окисленной, так и в восстановленной формах. [19]
Рассмотрим теперь некоторые примеры каталитических функций ионов, когда ион непосредственно взаимодействует с молекулами или ионами субстрата. Большую группу каталитически активных комплексов представляют такие соединения, в которых присоединяемые группы сами участвуют в реакции. [20]
 |
Максимальные поглощения н медные числа комплексов белков. [21] |
Как могут белки осуществлять свои каталитические функции. [22]
В некоторых случаях ингибитор прекращает каталитическую функцию фермента путем присоединения к активному центру. В этом случае говорят, что происходит конкурентное ингибиро-вание. Если место активного центра и место присоединения ингибитора расположены на разных участках поверхности фермента, то говорят о неконкурентном ингибировании. [23]
Активирующее действие гидроокиси меди на каталитическую функцию смеси гидроокисей марганца и кобальта привело его к выводу, что гидроокись меди является аналогом активной группы фермента. [24]
Металл образует каталитическую единицу с качественно новыми каталитическими функциями. Функции, свойственные этой самостоятельной единице, могут очень сильно отличаться от функций свободного иона. К этой группе относятся комплексы типа металлоферментов, содержащие белок: каталаза, карбоангидраза, хлорофилл и др. Функции, свойственные этим комплексам, совершенно отсутствуют или слабо выражены у соответствующих свободных ионов. [25]
Такие ферменты, идентичные по своей каталитической функции, но различные по другим молекулярным характеристикам, называются изоэнзимами или изозимами. Образование дублирующих друг друга ферментных белков связано с существенными затратами, но это обеспечивает клетке возможность специфической и точной регуляции систем, содержащих одинаковые этапы. Существование изоэнзимов, различающихся по конечному назначению, составляет одно из важных условий динамической организованности метаболизма. Конечная функция или назначение фермента становится существенным дополнением к его непосредственной функции. Существование различных молекулярных форм ферментов, аналогичных по своей специфической основной функции, но различных по конечному назначению в физиологическом отношении, является одним из важнейших условий нормального метаболизма клетки. Химические сигналы в клетке могут приниматься избирательно, и таким образом создается весьма точно действующая система строго направленных каналов связи для управления обменом веществ на основе информации о внутри - и внеклеточной химической среде. [26]
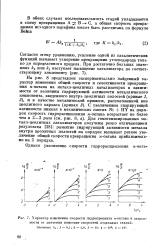 |
Характер изменения скорости гидрокрекинга н-октана в записи-моста от значения констант скоростей отдельных стадии. Значения ft, . 1 - 0 1. 2 - 1 0. 3 - 10. 4 - 10. 5 - 103. [27] |
Согласно этому уравнению, усиление одной из каталитических функций вызывает ускорение превращения углеводорода толь ко до определенного предела. [28]
В ряде случаев фермент может выполнять свою каталитическую функцию только в присутствии низкомолекулярных органических соединений - коферментов. Так, ферментативные процессы окисления и восстановления в организме происходят только при участии никотинамидных коферментов ( сокращенно НАД), имеющих строение, обеспечивающее перенос двух атомов водорода. [29]
 |
Переходное состояние комплекса алкогольдегидрогеназы при восстановлении ацетальдегида НАД-Н. [30] |
Страницы: 1 2 3 4