Термодинамическая функция - вещество
Cтраница 1
Термодинамические функции веществ в стандартном состояний называют стандартными и отмечают символом о - ДЯ, S, С р, AG, А / 70; их приводят в так называемых стандартных термодинамических таблицах. [1]
Термодинамические функции веществ в конденсированных состояниях, в отличие от термодинамических функций газов, в настоящее время не могут быть вычислены теоретически и определяются на основании результатов калориметрических измерений их теплоемкости или изменения энтальпии, а также теплот фазовых и полиморфных превращений от 0 К до рассматриваемой области температур. [2]
Термодинамические функции веществ, рассматриваемых в настоящей главе, были вычислены без учета межмолекулярного взаимодействия по постоянным, принятым в предыдущем параграфе, и приведены в табл. 1 - 6 II тома Справочника. Для четырех газов ( О, О, О2, О1) расчеты выполнены до 20 000 К, для двух остальных ( О - и О3) - до 6000 К. [3]
Термодинамические функции веществ, рассматриваемых в настоящей главе, в состоянии идеального газа были вычислены на основании молекулярных постоянных, принятых в предыдущем параграфе, и приведены в табл. 130 - 137, 142, 143, 148, 149, 156, 161, 162, 169 II тома настоящего Справочника. Для четырех газов ( С, С, СО, СО) расчеты выполнены до 20 000 К, для остальных - до 6000 К. [4]
Термодинамические функции веществ, рассматриваемых в настоящей главе, для состояния идеального газа были вычислены в интервале температур от 293 15 до 6000 К по молекулярным постоянным, принятым в предыдущем параграфе. [5]
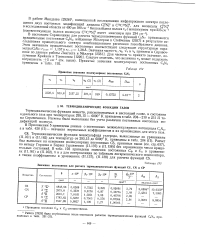 |
Значения постоянных для расчета термодинамических функций CS, CN и СР. [6] |
Термодинамические функции веществ, рассматриваемых в настоящей главе, в состоянии идеального газа при температурах 293 15 - 6000 К приведены в табл. 204 - 210 и 231 II тома Справочника. Расчеты были выполнены без учета различия постоянных изотопных модификаций молекул. [7]
Термодинамические функции вещества Р ( р, Т, х (), Е ( р, Т, jc -) даны в гл. [8]
Определение термодинамических функций веществ в твердом и жидком состояниях при высоких температурах на основании теоретических расчетов практически невозможно также вследствие отсутствия каких-либо надежных методов расчета температур и теплот фазовых переходов и теплоемкостей веществ в жидком состоянии. [9]
Точность расчета термодинамических функций веществ в твердом и жидком состояниях при высоких температурах определяется точностью всех исходных термодинамических величин, использованных для расчета, а именно - энтальпии и энтропии при 298 К, данных по теплоемкости веществ выше 298 К ( или данных по изменению энтальпии Нт - Я2Й8 15), величин температур и теплот фазовых переходов. [10]
Поэтому вычисление таблиц термодинамических функций веществ в твердом и жидком состояниях в настоящее время может быть проведено только на основании результатов экспериментальных измерений теплоемкости и теплот фазовых переходов с использованием соотношений, основанных на третьем законе термодинамики. [11]
Если возникает необходимость нахождения термодинамических функций веществ в состояниях реального газа, жидкости, твердом, то возможен переход на основе приведенных в гл. [12]
 |
Схема установки для изучения кинетики фотохимического разложения Н2О2. [13] |
Перед проведением работы следует по термодинамическим функциям веществ ( см. справочник) рассчитать тепловые эффекты элементарных стадий реакции и оценить принципиальную возможность их осуществления. [14]
 |
Схема установки для изучения кине-тики фотохимического разложения Н2О2. [15] |
Страницы: 1 2 3 4