Азеотропизм
Cтраница 1
Азеотропизм - явление весьма распространенное. Около 50 % всех систем, для которых изучено в настоящее время равновесие жидкость - пар, обладает азеотропиз-мом. [1]
Азеотропизм, если он свойствен данной системе, наблюдается в целой области параметров. [2]
Азеотропизм, как свойство системы, наблюдается в целом интервале параметров. Составы азеотропных смесей меняются с изменением температуры и давления. В некоторых системах азеотропы изменяют свои составы от оси одного чистого компонента до оси другого чистого компонента. [3]
Предсказание азеотропизма в трехкомпонентных система с ломошью выведенных соотношений производится следующим образом. По данным о равновесии или по данным о составе азеотропа рассчитываются конста. Далее, пользуясь неравенствами ( 156), ( 157) и ( 158), определяется т ran экстремума, - после чего то уравнению ( 154) определяется давление пара в экстремальной точке. [4]
Появление азеотропизма связано с наличием у некоторых систем особенностей в равновесии жидкость - газ. [5]
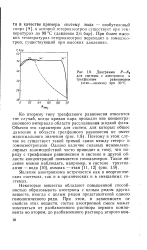 |
Диаграмма Р - JVa. [6] |
Явление азеотропизма встречается как в неорганических системах, так и в органических и в смешанных системах. [7]
Предсказание азеотропизма в трехкомпонентньгх системах с помощью выведенных соотношений производится следующим образом. По данным о равновесии или по данным о составе азеотропа рассчитываются конста. [8]
Исследование азеотропизма бинарных систем имеет большое-не только теоретическое, но и практическое значение, так как получение многих ценных продуктов органического синтеза связано с разделением азеотропных смесей. [9]
Область существования азеотропизма зависит от природы системы. В одних случаях азеотропные смеси могут образовываться во всей области существования равновесия жидкость - газ вплоть до критических параметров, в других - только в некотором интервале параметров. Точно это можно определить совместным решением уравнений (2.54), (2.55) и уравнения состояния, которому подчиняется данная система. В общем виде этот вопрос, как известно, пока не решается. [10]
Когда область азеотропизма заканчивается не на критической кривой, но при параметрах, достаточно близких к критическим параметрам наиболее летучего компонен-на, наличие минимума на изотерме и - N2 для газовой фазы может привести к образованию двойной критической точки. [11]
Системы с азеотропизмом при высоких давлениях, особенно в критической и закритической областях, были изучены до последнего времени очень мало. [12]
Если область существования азеотропизма Мала и заканчивается тангенциальным азеотропом на оси одного из чистых компонентов далеко от критической точки, то минимум на кривой и - Ni для газовой фазы может, по-видимому, постепенно сглаживаться и исчезнуть совсем. Минимум может, вероятно, и сохраниться в области температур, значительно превышающих температуру тангенциального азеотропа. [13]
Распространенность систем с азеотропизмом заставляет взглянуть на них с более общей точки зрения. Учение о фазовых равновесиях и объемных соотношениях, учение о критических явлениях не могут претендовать на полноту, если не изучены особенности поведения такого рода систем, тем более, что они составляют, как уже сказано, почти половину всех известных. [14]
Большинство растворов с азеотропизмом образуют положительные хазеотропы. Их сейчас известно большое количество. Гораздо реже встречаются системы с отрицательными отклонениями от идеальности. В системах с отрицательными отклонениями от идеальности часто наблюдаются явления ассоциации. Они вообще характеризуются ( за редким исключением) сильными межмолекулярными взаимодействиями. [15]
Страницы: 1 2 3 4