Диссоциация - фенол
Cтраница 1
Диссоциация фенолов характеризуется очень большим положительным значением ДЯ и лишь несколько большим отрицательным значением ГА5 ( для C6HsOH ГД5 - 33 3 кДж / моль); таким образом, и здесь, как и для кислот, основным фактором является энтропийный; потеря в энтропии тем меньше, чем больше делокализован отрицательный заряд в анионе и, следовательно, чем меньше сольватирован анион. В конечном итоге, чем более заместитель стабилизирует анион, тем больше константа диссоциации соответствующего соединения по сравнению с незамещенным. [1]
 |
Константы Гамметта и рКа замещенных бензойных кислот [ 99. [2] |
При диссоциации фенолов и анилинов, замещенных в ядре на группу триметиламмония, не обладающую резонансным эффектом, жета-изомер ведет себя как более сильная кислота. Если же заместитель - сульфонильная группа или остаток сульфоновой кислоты, то более сильной кислотой становится пара-изомер. [3]
Образующиеся при диссоциации фенолов ионы водорода Н взаимодействуют с ионами гидроксила из воды, что приводит к соответствующему сдвигу равновесия процесса диссоциации Однако, поскольку концентрация ионов ОН - в воде очень малаг то в отсутствие щелочи этот сдвиг незначителен. [4]
В условиях жидкофазного алкилирования аллиловым спиртом возможность диссоциации фенолов увеличивается, при этом растет концентрация фенолят-ионов, и, следовательно, растет вероятность образования продуктов О-аллилирования ( образования аллиловых эфиров крезолов), способных к дальнейшим превращениям. На количество образующихся аллиловых эфиров фенолов должны оказывать влияние три фактора: кислотность фенола, кислотность катализатора и устойчивость аллиловых эфиров в условиях опыта. По нашим данным, решающую роль в образовании аллиловых эфиров при жидкофазном алкилировании играет кислотность катализатора. [5]
Такая величина р значительно более положительна, чем для диссоциации фенолов в воде ( р 2 11), и с очевидностью доказывает, что переходное состояние имеет в высокой степени карбанионный характер. [6]
Такое прямое полярное сопряжение, однако, позволяет использовать диссоциацию фенолов в воде для определения ряда новых, альтернативных значений констант о для n - NO2 и других сходных электроноакцепторных заместителей; эти новые значения могут быть затем использованы для рассмотрения реакций, в которых может иметь место прямое сопряжение. [7]
Авторы полагают, что такой характер зависимости связан с диссоциацией фенола в органической фазе. [8]
Если в сточной воде содержатся щелочные примеси, то степень диссоциации фенолов возрастает, а следовательно, снижается полнота обесфеноливания воды. [9]
Введение нитрогруппы в орто - и пара-положения значительно повышает константу диссоциации фенола; меньший ацидифицирующий эффект оказывает мета-нитрогруппа. [10]
Введение нитрогруппы в орто - и пара-положения значительно повышает константу диссоциации фенола; меньший ацидифи-цирующий эффект оказывает мета-нитрогруппа. [11]
Роль щелочи в процессе обесфеноливания сводится к удалению ионов Н, образующихся при диссоциации фенолов и смещающих равновесие в процессе обесфеноливания в сторону снижения концентрации фенолов в водной фазе. [12]
Точно так же и концентрация иона фенолята в Кислом растворе очень мала, поскольку диссоциация фенола сильно подавлена. [13]
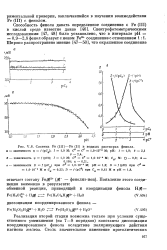 |
Система Fe ( III - Fe ( II в водных растворах фенола. о - зависимость р / ( рС. I 1 0 М. С Сг 1 0 - КГ М. рН. 1 - 1 9. г - 2 1. [14] |
Реализация второй стадии возможна только при условии существенного уменьшения ( на 7 - 8 порядков) константы диссоциации координированного фенола вследствие поляризующего действия катиона железа. [15]
Страницы: 1 2 3